3.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物.请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是( )
| A. | ZnC2水解生成乙烷(C2H6 ) | B. | Al4C3水解生成丙炔(C3H4) | ||
| C. | Mg2C3水解生成丙炔(C3H4) | D. | Li2C2水解生成乙烯(C2H4) |
2. 中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
 中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )
中国研制成功的全球唯一的治疗疟疾特效药--青蒿素,是数亿外国人眼中的“中国神药”,结构如图所示.目前售价每克225美元,世界年产量15吨,是需求量的十分之一,供不应求.下列关于青蒿素的说法正确的是( )| A. | 是一种烃 | B. | 属于高分子化合物 | ||
| C. | 属于芳香族化合物 | D. | 分子式是C15H22O5 |
1.A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1.E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同.

试回答:
(1)元素E在元素周期表中的位置是第三周期ⅣA族.
(2)与元素D离子所含电子数和质子数均相同的微粒是NH4+ (或H3O+).
(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的为H2SiO3.若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:ⅠHNO3,ⅡNa2SiO3,观察到的实验现象是中出现白色胶状沉淀.
(4)由以上五种元素组成的中学常见的物质,其组成和结构信息如下表:
①a含有的化学键有离子键、共价键;
②b与c反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.

试回答:
(1)元素E在元素周期表中的位置是第三周期ⅣA族.
(2)与元素D离子所含电子数和质子数均相同的微粒是NH4+ (或H3O+).
(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的为H2SiO3.若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:ⅠHNO3,ⅡNa2SiO3,观察到的实验现象是中出现白色胶状沉淀.
(4)由以上五种元素组成的中学常见的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1:1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
18.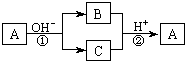 A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是
( )
 A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如图的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
| A. | X元素可能为Al | B. | X元素一定为非金属元素 | ||
| C. | 反应①和②互为可逆反应 | D. | 反应①和②不可能都为氧化还原反应 |
17.某元素的一种核素X的质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是( )
| A. | $\frac{a}{A+m}$(A-N+m)mol | B. | $\frac{a}{Am}$(A-N)mol | C. | $\frac{a}{A+m}$(A-N)mol | D. | $\frac{a}{A}$(A-N+m)mol |
16.下列离子方程式中书写不正确的是( )
0 168073 168081 168087 168091 168097 168099 168103 168109 168111 168117 168123 168127 168129 168133 168139 168141 168147 168151 168153 168157 168159 168163 168165 168167 168168 168169 168171 168172 168173 168175 168177 168181 168183 168187 168189 168193 168199 168201 168207 168211 168213 168217 168223 168229 168231 168237 168241 168243 168249 168253 168259 168267 203614
| A. | 少量二氧化硫与苛性钠溶液反应:SO2+2OH-=SO32-+H2O | |
| B. | 过量稀盐酸加入纯碱中:CO32-+2H+=H2O+CO2↑ | |
| C. | 铜粉与稀硫酸溶液反应:Cu+2H+=Cu2++H2↑ | |
| D. | 在氯化铝溶液中滴加过量的氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
 .
.

 .
.