15.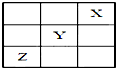 元素X、Y、Z在周期表中的相对位置如图所示:已知Y元素基态原子的外围电子排布为ns(n-1)np(n+1),则下列说法错误的是( )
元素X、Y、Z在周期表中的相对位置如图所示:已知Y元素基态原子的外围电子排布为ns(n-1)np(n+1),则下列说法错误的是( )
 元素X、Y、Z在周期表中的相对位置如图所示:已知Y元素基态原子的外围电子排布为ns(n-1)np(n+1),则下列说法错误的是( )
元素X、Y、Z在周期表中的相对位置如图所示:已知Y元素基态原子的外围电子排布为ns(n-1)np(n+1),则下列说法错误的是( )| A. | X元素所在周期中所含非金属元素最多 | |
| B. | Y元素在周期表的第3周期ⅥA族 | |
| C. | Y元素基态原子的价电子排布为4s24p4 | |
| D. | Z元素基态原子的核外电子排布式为1s22s22p63s23p63d104s24p3 |
14.HBr气体的热分解温度比HI热分解温度高的原因是( )
| A. | HBr分子中的键长比HI分子中的键长短,键能大 | |
| B. | HBr分子中的键长比HI分子中的键长长,键能小 | |
| C. | HBr的相对分子质量比HI的相对分子质量小 | |
| D. | HBr分子间作用力比HI分子间作用力大 |
13.下列说法正确的是( )
| A. | 同一原子中,2p、3p、4p能级的轨道数依次增多 | |
| B. | 电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则 | |
| C. |  表示的原子能量处于最低状态 表示的原子能量处于最低状态 | |
| D. | 在离核最近区域内运动的电子能量最低 |
12.下列化合物中,含有非极性共价键的离子化合物是( )
| A. | C2H4 | B. | CaCl2 | C. | Na2O2 | D. | NH4NO3 |
10.某元素质量数51,中子数28,其基态原子未成对电子数为( )
| A. | 4 | B. | 1 | C. | 2 | D. | 3 |
9.某基态原子的价电子排布式为4s24p1,则下列说法错误的是( )
| A. | 该元素在周期表中的位置是第4周期第ⅢA族 | |
| B. | 该元素原子核外有4个电子层 | |
| C. | 该元素原子最外层共有3个电子 | |
| D. | 该元素基态原子的电子排布式为[Ar]4s24p1 |
7.常温下,下列有关溶液的说法不正确的是( )
| A. | pH=3的二元弱酸H2R溶液与 pH=11的NaOH溶液混合后,混合液的pH等于7,则混合液中c(R2-)>c(Na+)>c(HR-) | |
| B. | 将0.2 mol/L的某一元弱酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液中存在:2c(OH-)+c(A-)=2c(H+)+c(HA) | |
| C. | 某物质的水溶液中由水电离出的c(H+)=1×10-amol/L,若a>7,则该溶液的pH为a或14-a | |
| D. | 相同温度下,0.2mol/L的醋酸溶液与0.1mol/L的醋酸溶液中c(H+)之比小于2:1 |
6.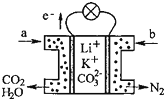 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图.下列说法正确的是( )
0 168070 168078 168084 168088 168094 168096 168100 168106 168108 168114 168120 168124 168126 168130 168136 168138 168144 168148 168150 168154 168156 168160 168162 168164 168165 168166 168168 168169 168170 168172 168174 168178 168180 168184 168186 168190 168196 168198 168204 168208 168210 168214 168220 168226 168228 168234 168238 168240 168246 168250 168256 168264 203614
 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图.下列说法正确的是( )| A. | 此电池在常温时也能工作 | |
| B. | 正极电极反应式为:O2+2CO2+4e-=2CO32- | |
| C. | CO32-向正极移动 | |
| D. | a为CH4,b为CO2 |
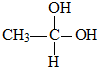 →CH3-CHO+H2O
→CH3-CHO+H2O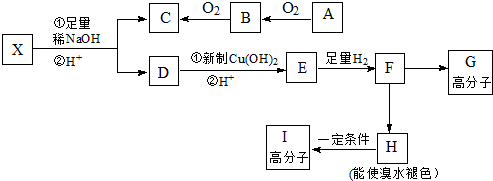
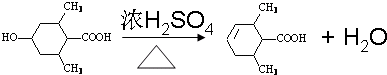
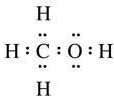 .
. ;
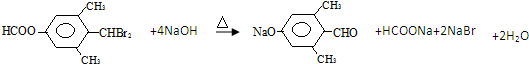
; ;
; ;
;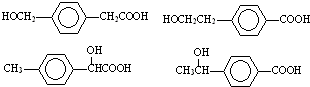 任意一种.
任意一种.