19.下列有机物的命名正确的是( )
| A. | 2─乙基戊烷 | B. | 2,3,3─三甲基丁烷 | ||
| C. | 2─甲基-3-丁醇 | D. | 2,3-二乙基-1-戊烯 |
18.A元素的最高正价和最低负价的绝对值之差为6,B元素和A元素的原子次外层都有8个电子,BA2在水溶液中电离出电子层结构相同的离子,则BA2是( )
| A. | MgF2 | B. | CaCl2 | C. | K2S | D. | Na2O |
17.A、B两元素为同一周期ⅡA族和ⅢA族元素,若A元素的原子序数为x,则B元素的原子序数可能为( )
①x+1 ②x+8 ③x+11 ④x+18 ⑤x+25 ⑥x+32.
①x+1 ②x+8 ③x+11 ④x+18 ⑤x+25 ⑥x+32.
| A. | ①②③④ | B. | ①③⑥ | C. | ①③⑤ | D. | ②④⑥ |
16.有aXn+和bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A. | a-b=n+m | B. | b-a=n+m | ||
| C. | 原子序数:Y>X | D. | 离子半径:Ym-<Xn+ |
15.元素的以下性质,随着原子序数递增不呈现周期性变化的是( )
0 167248 167256 167262 167266 167272 167274 167278 167284 167286 167292 167298 167302 167304 167308 167314 167316 167322 167326 167328 167332 167334 167338 167340 167342 167343 167344 167346 167347 167348 167350 167352 167356 167358 167362 167364 167368 167374 167376 167382 167386 167388 167392 167398 167404 167406 167412 167416 167418 167424 167428 167434 167442 203614
| A. | 化合价 | B. | 原子半径 | ||
| C. | 元素的金属性和非金属性 | D. | 相对原子质量 |
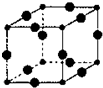 Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.
Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的巨大作用.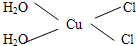 .
. 为测定碳酸钙的纯度(杂质SiO2),学生设计了如下几个实验方案,请回答每个方案中的问题.(相对原子质量:C=12 O=16 Ca=40)
为测定碳酸钙的纯度(杂质SiO2),学生设计了如下几个实验方案,请回答每个方案中的问题.(相对原子质量:C=12 O=16 Ca=40)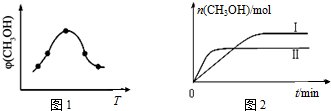
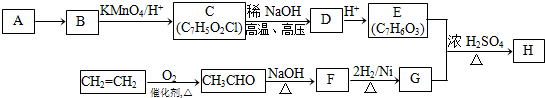
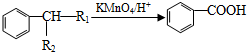 (-R1、-R2表示氢原子或烃基);
(-R1、-R2表示氢原子或烃基);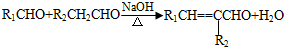 ;
;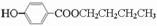 .
.