11.某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol•L-1)随反应时间(min)的变化情况如表所示.
根据上述数据,完成下列填空:
(1)在实验1中,反应在10~20min时间内A的平均反应速率为0.013mol•L-1•min-1
(2)在实验2中,A的初始浓度c2=1.0mol•L-1.
(3)设实验3的反应速率为v3.,实验1的反应速率为v1,则v3>vl(填“>”、“=“或“<”).
(4)比较实验4和实验1,可推测该反应是吸热(填“吸热”或“放热”)反应.理由是温度升高时,平衡向右移动.
| 实验 序号 | 浓度 时间 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,反应在10~20min时间内A的平均反应速率为0.013mol•L-1•min-1
(2)在实验2中,A的初始浓度c2=1.0mol•L-1.
(3)设实验3的反应速率为v3.,实验1的反应速率为v1,则v3>vl(填“>”、“=“或“<”).
(4)比较实验4和实验1,可推测该反应是吸热(填“吸热”或“放热”)反应.理由是温度升高时,平衡向右移动.
4. 短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为.
短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为.
请回答下列问题:
(1)Z元素在元素周期表中的位置是第三周期第VA族.
(2)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(元素符号表示).
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为HNO3>H3PO4>H2CO3(用化学式表示)
(4)用电子式表示WY2的形成过程: .
.
(5)写出W单质与浓硫酸反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
0 163886 163894 163900 163904 163910 163912 163916 163922 163924 163930 163936 163940 163942 163946 163952 163954 163960 163964 163966 163970 163972 163976 163978 163980 163981 163982 163984 163985 163986 163988 163990 163994 163996 164000 164002 164006 164012 164014 164020 164024 164026 164030 164036 164042 164044 164050 164054 164056 164062 164066 164072 164080 203614
 短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为.
短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为.| W | X | Y |
| Z |
(1)Z元素在元素周期表中的位置是第三周期第VA族.
(2)X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O(元素符号表示).
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序为HNO3>H3PO4>H2CO3(用化学式表示)
(4)用电子式表示WY2的形成过程:
 .
.(5)写出W单质与浓硫酸反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O.
 ,H2O中含有的化学键为极性键(离子键、极性键、非极性键)
,H2O中含有的化学键为极性键(离子键、极性键、非极性键)
 .
.
 .
.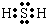 ;
; 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题. 为原料,按以下步骤从合成
为原料,按以下步骤从合成  (部分试剂和反应条件已略去).
(部分试剂和反应条件已略去).
 .
. $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. 有多种同分异构体,其中既能发生水解反应,又能发生银镜反应的有机物共有8种.
有多种同分异构体,其中既能发生水解反应,又能发生银镜反应的有机物共有8种. .
.