3. 室温下,将x mol•L-1NaOH溶液滴10mL 0.1mol•L-1的醋酸溶液中,溶液的温度和pH变化如图所示.下列说法正确的是( )
室温下,将x mol•L-1NaOH溶液滴10mL 0.1mol•L-1的醋酸溶液中,溶液的温度和pH变化如图所示.下列说法正确的是( )
 室温下,将x mol•L-1NaOH溶液滴10mL 0.1mol•L-1的醋酸溶液中,溶液的温度和pH变化如图所示.下列说法正确的是( )
室温下,将x mol•L-1NaOH溶液滴10mL 0.1mol•L-1的醋酸溶液中,溶液的温度和pH变化如图所示.下列说法正确的是( )| A. | x=0.1 | |
| B. | 滴定过程中应该选择甲基橙作为指示剂 | |
| C. | c点对应的溶液中水的电离程度最大 | |
| D. | b点对应的溶液中c(H+)=(OH-)=C(Na+)=c(CH3COO-) |
2. 已知:pKa=-lgKa,25℃时,H2A的pKal=1.85,pKa2=7.19.常温下,用0.1mol•L-1NaOH溶液滴定20mL 0.1mol•L-1H2A溶液的滴定曲线如图所示.下列说法正确的是( )
已知:pKa=-lgKa,25℃时,H2A的pKal=1.85,pKa2=7.19.常温下,用0.1mol•L-1NaOH溶液滴定20mL 0.1mol•L-1H2A溶液的滴定曲线如图所示.下列说法正确的是( )
 已知:pKa=-lgKa,25℃时,H2A的pKal=1.85,pKa2=7.19.常温下,用0.1mol•L-1NaOH溶液滴定20mL 0.1mol•L-1H2A溶液的滴定曲线如图所示.下列说法正确的是( )
已知:pKa=-lgKa,25℃时,H2A的pKal=1.85,pKa2=7.19.常温下,用0.1mol•L-1NaOH溶液滴定20mL 0.1mol•L-1H2A溶液的滴定曲线如图所示.下列说法正确的是( )| A. | a点所得溶液中:V0=10 mL | |
| B. | b点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-) | |
| C. | c点所得溶液中:c(A2-)=c(HA-) | |
| D. | d点所得溶液中A2-水解平衡常数Khl=10-7.19 |
1.以下表示氦原子结构的化学用语中,对电子运动状态描述最详尽的是( )
| A. | He | B. |  | C. | 1s2 | D. | 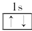 |
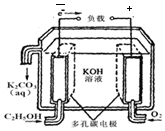
6. 一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg $?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg $?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
 一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg $?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg $?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )| A. | 放电时,镁电极为负极,发生氧化反应 | |
| B. | 放电时,正极的电极反应式为Fe3S4+8e-=3Fe+4S2- | |
| C. | 充电时,S2-从阴离子交换膜左侧向右侧迁移 | |
| D. | 充电时转移2mol电子,阴极质量减少32g |
4. 0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.
0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.
①在图中a表示向稀醋酸中不断加水,b表示向稀醋酸中慢慢滴加0.10mol•Lˉ1的稀氢氧化钠溶液.a中醋酸电离百分率的变化图线已画出,请你图中画出b过程中醋酸电离百分率的变化图线.
②一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
求该温度下醋酸的电离常数1.0×10-5.当醋酸浓度为0.1mol•L-1时,则电离度为1%.
 0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.
0.10mol•L-1的稀醋酸中存在着平衡:CH3COOH?CH3COOˉ+H+.①在图中a表示向稀醋酸中不断加水,b表示向稀醋酸中慢慢滴加0.10mol•Lˉ1的稀氢氧化钠溶液.a中醋酸电离百分率的变化图线已画出,请你图中画出b过程中醋酸电离百分率的变化图线.
②一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| 醋酸浓度(mol•L-1) | 1 | 0.1 | 0.01 |
| pH值 | 2.50 | 3.00 | 3.50 |
1.下列有关化学用语书写正确的是( )
| A. | 碳酸氢钠的水解:HCO3-+H2O=H3+O+CO32- | |
| B. | 14g乙烯燃烧生成液态水产生b kJ热量,则表示其燃烧热的热化学方程式为:C2H4(g)+3O2(g)═2H2O(g)+2CO2(g)△H=-2b kJ•mol-1 | |
| C. | 用两根铜棒电解盐酸:2H++2Cl-$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑ | |
| D. | 在酸性碘化亚铁溶液中通入少量氧气:4I-+O2+4H+=2I2+2H2O |
20.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
0 163513 163521 163527 163531 163537 163539 163543 163549 163551 163557 163563 163567 163569 163573 163579 163581 163587 163591 163593 163597 163599 163603 163605 163607 163608 163609 163611 163612 163613 163615 163617 163621 163623 163627 163629 163633 163639 163641 163647 163651 163653 163657 163663 163669 163671 163677 163681 163683 163689 163693 163699 163707 203614
| A. | 常温下,22.4LNH3与氧气完全反应生成NO时,转移的电子数小于5NA | |
| B. | 在1mol重甲基(-CD3)中含有的电子数为9NA | |
| C. | 在电解食盐水的实验中,若电解后溶液总体积为1L,阴极析出的气体的分子数为0.5NA,电解后溶液的pH为12 | |
| D. | 一定条件下3mol SO2和1 molO2 混合在密闭容器中充分反应后的分子总数为3NA |
 取一定量的铁粉与2mol•L-1稀硝酸400mL反应,反应后硝酸和铁均无剩余(铁只显+2价),且硝酸的还原产物只有NO.(不考虑溶液体积的变化)
取一定量的铁粉与2mol•L-1稀硝酸400mL反应,反应后硝酸和铁均无剩余(铁只显+2价),且硝酸的还原产物只有NO.(不考虑溶液体积的变化)