17.乙醇分子中不同的化学键如图:关于乙醇在各种不同反应中断裂键的说明不正确的是( ) 

| A. | 和金属钠反应时键④断裂 | |
| B. | 和氢溴酸反应时键②断裂 | |
| C. | 和浓硫酸共热140℃时键③或键④断裂;170℃时键①③断裂 | |
| D. | 在Ag催化下和O2反应键②④断裂 |
16.某有机物的结构如图所示,下列说法正确的是( )
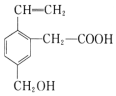

| A. | 有机物的分子式为C11H14O3 | |
| B. | 有机物中含有4种不同的官能团 | |
| C. | 0.5 mol 该有机物与足量NaOH溶液反应,消耗NaOH 1mol | |
| D. | 0.5 mol 该有机物与足量金属钠反应,能生成标准状况下的氢气11.2L |
15.在容积不变的某2L的密闭容器中,充入H2与N2的混合气体共5mol,在一定条件下,5min后反应达到平衡,此时容器内的压强是反应前的$\frac{4}{5}$.则下列说法不正确的是( )
| A. | 从反应开始到平衡时,用H2表示的平均反应速率为0.15 mol•L-1•min-1 | |
| B. | 反应达到平衡时,NH3的物质的量浓度是0.5 mol•L-1 | |
| C. | 反应达到平衡时,N2和H2的物质的量之比一定为1:3 | |
| D. | 反应达到平衡时,反应物和生成物的总的物质的量之比为3:1 |
14.下列关系正确的是( )
| A. | 沸点:戊烷>2-甲基丁烷>乙二醇 | |
| B. | 密度:硝基苯>H2O>汽油 | |
| C. | 等质量的物质燃烧耗O2量:乙烯>乙炔>甲烷 | |
| D. | 等物质的量物质燃烧耗O2量:丙烷>环丙烷>2-丙醇 |
13.现有四组混合物:①乙酸乙酯和乙酸钠溶液 ②甲醇和甘油 ③葡萄糖和淀粉的混合液 ④溴化钠和单质溴的水溶液,分离以上各混合物的正确方法依次是( )
| A. | 分液、萃取、蒸馏、渗析 | B. | 分液、蒸馏、渗析、萃取 | ||
| C. | 萃取、蒸馏、分液、萃取 | D. | 蒸馏、萃取、渗析、萃取 |
12.下列说法正确的是( )
| A. | 向苯酚钠溶液中通入CO2可制得苯酚,并得到碳酸钠 | |
| B. | 将铁屑、溴水、苯混合可制得溴苯 | |
| C. | 实验时不小心沾到手上的苯酚可用氢氧化钠溶液洗掉 | |
| D. | 用醋酸溶液洗涤沾附在暖水瓶内壁上水垢的过程中发生了复分解反应 |
10. 如图是Ca(OH)2在温度分别为T1、T2时的沉淀溶解平衡曲线[图中浓度单位为mol•L-1,温度为T1时Ca(OH)2的Ksp=4×10-6,$\root{3}{4}$≈1.6].下列说法正确的是( )
如图是Ca(OH)2在温度分别为T1、T2时的沉淀溶解平衡曲线[图中浓度单位为mol•L-1,温度为T1时Ca(OH)2的Ksp=4×10-6,$\root{3}{4}$≈1.6].下列说法正确的是( )
 如图是Ca(OH)2在温度分别为T1、T2时的沉淀溶解平衡曲线[图中浓度单位为mol•L-1,温度为T1时Ca(OH)2的Ksp=4×10-6,$\root{3}{4}$≈1.6].下列说法正确的是( )
如图是Ca(OH)2在温度分别为T1、T2时的沉淀溶解平衡曲线[图中浓度单位为mol•L-1,温度为T1时Ca(OH)2的Ksp=4×10-6,$\root{3}{4}$≈1.6].下列说法正确的是( )| A. | 温度:T1<T2 | |
| B. | 温度为T1时,P点分散系中分散质粒子直径均小于1nm | |
| C. | Q点的溶液中c(OH-)约为0.0125mol•L-1 | |
| D. | 加水稀释时溶液碱性减弱,Z点溶液可转化为Q点溶液 |
9.为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250mL溶液.设计了以下两种实验方案:
方案I:取25.00mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取25.00mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定.(5SO32-+2MnO4-+6H+→5SO42-+2Mn2++3H2O)
实验中所记录的数据如表:
(1)配制250mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和电子天平、250mL的容量瓶.
(2)操作I为过滤操作Ⅱ为干燥
(3)方案I中如何判别加入的氯化钡已经过量静置分层后,向上清液中加入盐酸酸化的氯化钡,不再产生沉淀,即已沉淀完全在方案Ⅱ中滴定终点的判断方法是加入最后一滴后溶液由无色变为紫色,且在半分钟内不褪.
(4)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为$\frac{6300a}{W}$%.(写成分数形式)
有同学模仿方案I,提出方案Ⅲ:取25.00mL上述溶液→加入足量的盐酸酸化的Ba(NO3)2溶液→操作I→洗涤→操作Ⅱ→称重,得到沉淀质量为m2 g 并用方案I的方法计算结果.
(5)根据方案Ⅲ,从理论上讲,下列说法正确的是bd(填序号)
a.方案I比方案Ⅲ的计算结果要低 b.方案I比方案Ⅲ的计算结果要高
c.m1=m2,方案I和方案Ⅲ的结果一样 d.方案Ⅲ不应根据方案I的方法计算
(6)上述实验中,由于操作错误所引起的实验误差分析正确的是ad(填序号).
a.方案I中如果没有洗涤操作,实验结果将偏小
b.方案I中如果没有操作Ⅱ,实验结果将偏大
c.方案Ⅲ中如果没有洗涤操作,实验结果将偏小
d.方案Ⅲ中如果没有操作Ⅱ,实验结果将偏大.
0 163471 163479 163485 163489 163495 163497 163501 163507 163509 163515 163521 163525 163527 163531 163537 163539 163545 163549 163551 163555 163557 163561 163563 163565 163566 163567 163569 163570 163571 163573 163575 163579 163581 163585 163587 163591 163597 163599 163605 163609 163611 163615 163621 163627 163629 163635 163639 163641 163647 163651 163657 163665 203614
方案I:取25.00mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取25.00mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定.(5SO32-+2MnO4-+6H+→5SO42-+2Mn2++3H2O)
实验中所记录的数据如表:
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| 待测溶液体积/mL | 25.00 | 25.00 | 25.00 | 25.00 |
| 滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
| 滴定管末读数/mL | 20.95 | 21.20 | 20.15 | 21.20 |
(2)操作I为过滤操作Ⅱ为干燥
(3)方案I中如何判别加入的氯化钡已经过量静置分层后,向上清液中加入盐酸酸化的氯化钡,不再产生沉淀,即已沉淀完全在方案Ⅱ中滴定终点的判断方法是加入最后一滴后溶液由无色变为紫色,且在半分钟内不褪.
(4)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为$\frac{6300a}{W}$%.(写成分数形式)
有同学模仿方案I,提出方案Ⅲ:取25.00mL上述溶液→加入足量的盐酸酸化的Ba(NO3)2溶液→操作I→洗涤→操作Ⅱ→称重,得到沉淀质量为m2 g 并用方案I的方法计算结果.
(5)根据方案Ⅲ,从理论上讲,下列说法正确的是bd(填序号)
a.方案I比方案Ⅲ的计算结果要低 b.方案I比方案Ⅲ的计算结果要高
c.m1=m2,方案I和方案Ⅲ的结果一样 d.方案Ⅲ不应根据方案I的方法计算
(6)上述实验中,由于操作错误所引起的实验误差分析正确的是ad(填序号).
a.方案I中如果没有洗涤操作,实验结果将偏小
b.方案I中如果没有操作Ⅱ,实验结果将偏大
c.方案Ⅲ中如果没有洗涤操作,实验结果将偏小
d.方案Ⅲ中如果没有操作Ⅱ,实验结果将偏大.
