6.下列表达正确的是( )
| A. | N2的电子式为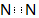 | B. | H2S的电子式可表示为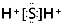 | ||
| C. | 用电子式表示Na2O的形成过程为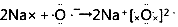 | D. | MgCl2的电子式为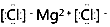 |
5. KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
 KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )| A. | KClO3和 KHSO3发生反应的氧化剂与还原剂的物质的量之 比为1:3 | |
| B. | 反应开始阶段速率逐渐增大可能是 c(H+)逐渐增高导致的 | |
| C. | 反应后期速率逐渐减小的主要原因是 c(ClO3 )、c(HSO3)降低 | |
| D. | 纵坐标为 v(HSO3-)时 v-t 的曲线与原图曲线完全吻合 |
4.下列说法错误的是( )
| A. | 乙烯使酸性高锰酸钾溶液、溴水褪色,原理相同 | |
| B. | 通过加成反应、取代反应都可以生成 CH3CH2Cl | |
| C. | 乙烯具有可燃性,在点燃前要验纯 | |
| D. | 乙烷中混有的乙烯可用溴水除去 |
3.设 NA 为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,33.6 L 氟化氢中含有氟原子的数目为 1.5NA | |
| B. | 常温常压下,7.0 g 乙烯与丙烯的混合物中含有氢原子的数目为NA | |
| C. | 50mL l8.4 mol/L 浓硫酸与足量铜微热反应,生成 SO2分子的数目为 0.46NA | |
| D. | 某密闭容器盛有0.lmolN2和0.3molH2,在一定条件下充分反应,转移电子的数 目为 0.6NA |
2.下列关于甲烷的性质叙述正确的是( )
| A. | 甲烷与氯气按物质的量之比l:l混合发生取代反应时,只生成CH3Cl和HCl | |
| B. | 甲烷可以与氯气发生取代反应,因此可以使氯水褪色 | |
| C. | 甲烷能够燃烧,在一定条件下会发生爆炸,因此它是矿井安全的重要威胁之一 | |
| D. | 甲烷完全燃烧的化学方程式为:2CH4+3O2$\stackrel{点燃}{→}$2CO+4H2O |
1.下列关于烷烃的叙述中不正确的是( )
| A. | 在烷烃分子中,所有的化学键都为单键 | |
| B. | 所有的烷烃在一定条件下都能与Cl2发生取代反应 | |
| C. | 随着碳原子数的增加,烷烃的熔、沸点逐渐升高 | |
| D. | 任何烷烃分子中碳氢原子个数之比都是相同的 |
7.0℃,101325Pa(称为标准状况)下,等质量的下列物质,所占体积最大的是( )
| A. | CO2 | B. | O2 | C. | H2O | D. | Na |
6.阿托酸是一种常用的医药中间体,其结构如图所示.下列关于阿托酸的说法正确的是( )

| A. | 分子式为C9H10O2 | |
| B. | 能发生取代、加聚、氧化等反应 | |
| C. | 不能与Na2CO3溶液反应放出气体 | |
| D. | 1 mol阿托酸最多能和5 mol Br2发生加成反应 |
5.如图,将铁棒和碳棒用导线连接后插入稀硫酸中,构成原电池.下列叙述不正确的是( )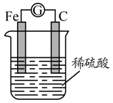

| A. | 电子从碳棒经导线流向铁棒 | B. | 铁棒是负极,碳棒是正极 | ||
| C. | 电池反应为:Fe+2H+=Fe2++H2↑ | D. | 碳棒上有气体放出,溶液c(H+)减小 |
4.有关化学用语正确的是( )
0 163414 163422 163428 163432 163438 163440 163444 163450 163452 163458 163464 163468 163470 163474 163480 163482 163488 163492 163494 163498 163500 163504 163506 163508 163509 163510 163512 163513 163514 163516 163518 163522 163524 163528 163530 163534 163540 163542 163548 163552 163554 163558 163564 163570 163572 163578 163582 163584 163590 163594 163600 163608 203614
| A. | 乙烯的结构简式:CH2CH2 | B. | 氮气的电子: | ||
| C. | 硅的原子结构示意图: | D. | 蔗糖的分子式:C6H12O6 |