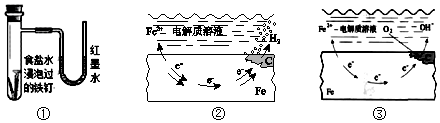
13.将纯水加热至较高温度,下列叙述正确的是( )
| A. | 水的离子积变大,c(H+)变大,呈酸性 | B. | 水的离子积不变,c(H+)不变,呈中性 | ||
| C. | 水的离子积变小,c(H+)变小,呈碱性 | D. | 水的离子积变大,c(H+)变大,呈中性 |
12.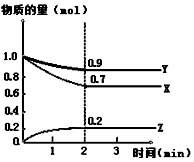 某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
 某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )
某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是( )| A. | 用X表示该化学反应速率比用Y表示的要快 | |
| B. | 该反应的化学方程式:3X+Y?2Z | |
| C. | 若在3min后,把Z从反应体系中分离,平衡不移动 | |
| D. | 反应开始至2min,Z的平均反应速率:0.1mol/(L•min) |
10.下列关于共价键与共价化合物的叙述中正确的是( )
①含金属元素的化合物一定不是共价化合物
②共价化合物中一定只含有共价键
③共价化合物中一定不含离子键
④含有共价键的化合物一定是共价化合物
⑤离子化合物中可能含有共价键.
①含金属元素的化合物一定不是共价化合物
②共价化合物中一定只含有共价键
③共价化合物中一定不含离子键
④含有共价键的化合物一定是共价化合物
⑤离子化合物中可能含有共价键.
| A. | ②③⑤ | B. | ②③④⑤ | C. | ②③④ | D. | ①②③⑤ |
9.下列有关海水综合利用的说法正确的是( )
| A. | 电解熔融的氯化镁可制备镁单质和氯气 | |
| B. | 从海水制食盐主要是通过化学变化完成 | |
| C. | 电解氯化铝可以制得铝单质和氯气 | |
| D. | 从海水中提取钠单质只发生物理变化 |
8.下列实验中,反应速率增大是由催化剂引起的是( )
| A. | 双氧水中加入少量MnO2,即可迅速放出气体 | |
| B. | 锌与稀硫酸反应中加入少量CuSO4溶液,反应放出H2的速率加快 | |
| C. | 固态FeCl3和固体NaOH混合后,加入水能迅速产生沉淀 | |
| D. | 在炭粉中加入KClO3,点燃时燃烧更为剧烈 |
7.下列关于有机化合物的说法正确的是( )
| A. | 乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色 | |
| B. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物数目相同 | |
| C. | 淀粉和纤维素是同分异构体 | |
| D. | 油脂的皂化反应属于加成反应 |
6.某化学科研小组研究电解饱和食盐水的相关内容.
Ⅰ.设计如下方案测定饱和食盐水的电解率.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]

方案一:将甲中A或B口的气体通入乙中的洗气瓶,通过测定洗气瓶D在电解前后质量变化来计算饱和食盐水的电解率.
(1)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)与导管口C相连的一极为B(填“A”或“B”).甲装置中产生NaOH的一极是铁棒(填“铁棒”或“碳棒”).
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
实验过程为:
a.电解几分钟后,量取10.00mL电解液(从含NaOH的一极取液),加入锥形瓶中.
b.向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液.
c.记录滴定三次所耗盐酸的体积如下:
(3)滴定时,边滴边摇动锥形瓶,直到溶液由红色变无色,并保持半分钟不褪色时停止滴定.
(4)若电解前饱和食盐水的物质的量浓度为5.4mol•L-1,则该食盐水的电解率表示为7.78%(用分数表示出来即可,不用化简).
(5)科研小组对比数据发现:方案一测得的电解率小于方案二的电解率,请分析可能的原因解生成的氯气不能完全被吸收.
0 163381 163389 163395 163399 163405 163407 163411 163417 163419 163425 163431 163435 163437 163441 163447 163449 163455 163459 163461 163465 163467 163471 163473 163475 163476 163477 163479 163480 163481 163483 163485 163489 163491 163495 163497 163501 163507 163509 163515 163519 163521 163525 163531 163537 163539 163545 163549 163551 163557 163561 163567 163575 203614
Ⅰ.设计如下方案测定饱和食盐水的电解率.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]

方案一:将甲中A或B口的气体通入乙中的洗气瓶,通过测定洗气瓶D在电解前后质量变化来计算饱和食盐水的电解率.
(1)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)与导管口C相连的一极为B(填“A”或“B”).甲装置中产生NaOH的一极是铁棒(填“铁棒”或“碳棒”).
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
实验过程为:
a.电解几分钟后,量取10.00mL电解液(从含NaOH的一极取液),加入锥形瓶中.
b.向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液.
c.记录滴定三次所耗盐酸的体积如下:
| 实验序号 | 盐酸体积(mL) |
| 第一次 | 20.90 |
| 第二次 | 21.00 |
| 第三次 | 21.10 |
(4)若电解前饱和食盐水的物质的量浓度为5.4mol•L-1,则该食盐水的电解率表示为7.78%(用分数表示出来即可,不用化简).
(5)科研小组对比数据发现:方案一测得的电解率小于方案二的电解率,请分析可能的原因解生成的氯气不能完全被吸收.


 .
.