3. 一定温度压强下,NO在某恒容密闭容器中分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示.下列说法正确的是( )
一定温度压强下,NO在某恒容密闭容器中分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示.下列说法正确的是( )
 一定温度压强下,NO在某恒容密闭容器中分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示.下列说法正确的是( )
一定温度压强下,NO在某恒容密闭容器中分解生成两种化合物,体系中各组分物质的量随时间变化曲线如图所示.下列说法正确的是( )| A. | 该反应是一个可逆反应 | B. | 反应后体系内压强增大 | ||
| C. | Y、Z的化学式分别是N2O、N2O3 | D. | Y、Z的化学式分别是N2O、NO2 |
2.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4L苯中含σ键数目为12NA | |
| B. | 常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA | |
| C. | 常温下,1.0L 0.1 mol•L-1 FeCl3溶液中,Fe3+离子数目为0.1NA | |
| D. | O3氧化NO 结合水洗可产生HNO3和O2,每生成1mol HNO3转移的电子数为6NA |
1.有关工业合成氨的说法正确的是( )
| A. | 使用催化剂的目的是提高反应物的转化率 | |
| B. | 循环使用N2、H2的目的是提高氨的产率 | |
| C. | 温度控制在500℃左右的目的是有利于化学平衡向正反应方向移动 | |
| D. | 高压下反应有利于增大反应速率,所以压强越高越好 |
20.某实验小组利用煤矸石主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO等提取Al(OH)3,首先需要用盐酸对煤矸石进行“酸浸”,为提高铝的浸出率,下列措施不合适的是( )
| A. | 提高盐酸的浓度 | B. | 搅拌反应物 | C. | 高温下酸浸 | D. | 粉碎煤矸石 |
19.下列说法中正确的是( )
| A. | 现向10mL浓度为0.1 mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中水的电离程度始终增大 | |
| B. | 保存Fe(NO3)2溶液时,应在其中加入稀HNO3以抑制Fe2+水解 | |
| C. | 将AlCl3溶液蒸干可得到固体AlCl3 | |
| D. | 向0.1 mol•L-1氨水中加入少量水,pH减小,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 |
18.下列叙述中正确的是( )
| A. | 因为水分子内含有氢键,所以水的沸点比硫化氢的沸点高 | |
| B. | N3-离子与CO2分子互为等电子体 | |
| C. | CHBrCl2分子中的碳原子为手性碳原子 | |
| D. | SO2和CO2均为直线形结构 |
16.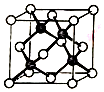 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )
 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )| A. | 冰晶胞内水分子间以共价键结合 | |
| B. | 晶体冰与金刚石晶体硬度都很大 | |
| C. | 冰分子间的氢键无方向性和饱和性 | |
| D. | 氢键存在导致冰晶胞与金刚石晶胞排列方式类似 |
15.被称为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,在其另一边镀二氧化锰)作为传导体.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为Zn+2MnO2+H2O═ZnO+2MnO(OH)下列说法不正确的是( )
0 163340 163348 163354 163358 163364 163366 163370 163376 163378 163384 163390 163394 163396 163400 163406 163408 163414 163418 163420 163424 163426 163430 163432 163434 163435 163436 163438 163439 163440 163442 163444 163448 163450 163454 163456 163460 163466 163468 163474 163478 163480 163484 163490 163496 163498 163504 163508 163510 163516 163520 163526 163534 203614
| A. | 该电池锌为负极,发生氧化反应 | |
| B. | 电池正极反应式为MnO2+e-+H2O═MnO(OH)+OH- | |
| C. | 当0.1mol Zn完全溶解时,电池外电路转移的电子个数约为1.204×1023 | |
| D. | 当该电池工作时,负极周围的pH值变大 |


