16.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1mol/L的硫酸溶液中含有的H+离子数为2NA | |
| B. | 常温下,11.2L甲烷气体含有的甲烷分子数为0.5NA | |
| C. | 22.4L NO2和CO2混合气体中含有的氧原子数为2NA | |
| D. | 标准状况下,18gH2O所含的氧原子数目为NA |
15.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构,下列说法正确的是( )
| A. | 原子最外层电子数:Z>Y>X | B. | 单质熔点:Y>Z>X | ||
| C. | 离子半径:X2->Z->Y+ | D. | 原子序数:X>Z>Y |
13.核素178O的原子核内的中子数与核外电子数之差是( )
| A. | 9 | B. | 8 | C. | 1 | D. | 17 |
12.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入100mL水中,所得溶液中c(Cl-)=c(I-) |
11.下列有关化学反应方向及其判据的说法中错误的是( )
| A. | 1 mol H2O在不同状态时的熵值:S[H2O(s)]<S[H2O(g)] | |
| B. | 凡是放热反应都是自发的,因为吸热反应都是非自发的 | |
| C. | CaCO3(s)?CaO(s)+CO2(g)△H>0 能否自发进行与温度有关 | |
| D. | 常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
10.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ•mol-1则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,则石墨比金刚石稳定 | |
| D. | 己知2C(s)+2O2(g)═2CO2(g)△H=a kJ•mol-1,2C(s)+O2(g)═2CO(g)△H=b kJ•mol-1,则a>b |
9.下列物质中,发生消去反应生成的烯烃只有一种的是( )
| A. | 2-丁醇 | B. | 2-戊醇 | C. | 2-甲基-2-丙醇 | D. | 2-甲基-2-丁醇 |
8.维生素C的结构简式为  ,有关它的叙述错误的是( )
,有关它的叙述错误的是( )
 ,有关它的叙述错误的是( )
,有关它的叙述错误的是( )| A. | 强还原性 | |
| B. | 易起氧化及加成反应 | |
| C. | 易溶于水 | |
| D. | 加热难分解,在碱性溶液中能稳定地存在 |
7.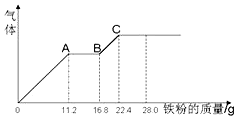 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
0 163065 163073 163079 163083 163089 163091 163095 163101 163103 163109 163115 163119 163121 163125 163131 163133 163139 163143 163145 163149 163151 163155 163157 163159 163160 163161 163163 163164 163165 163167 163169 163173 163175 163179 163181 163185 163191 163193 163199 163203 163205 163209 163215 163221 163223 163229 163233 163235 163241 163245 163251 163259 203614
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 原溶液中H2SO4浓度为4mol•L-1 | |
| B. | 图中,AB段的反应为2Fe3++Fe=3Fe2+,A点的溶质为Fe(NO3)3 | |
| C. | 原混合液中NO3-的物质的量为0.4mol | |
| D. | 图中,OA段产生是NO,BC段产生的气体是氢气 |
 研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题:
研究化学反应中的能量变化有重要意义.请根据学过的知识回答下列问题: