0 16021 16029 16035 16039 16045 16047 16051 16057 16059 16065 16071 16075 16077 16081 16087 16089 16095 16099 16101 16105 16107 16111 16113 16115 16116 16117 16119 16120 16121 16123 16125 16129 16131 16135 16137 16141 16147 16149 16155 16159 16161 16165 16171 16177 16179 16185 16189 16191 16197 16201 16207 16215 203614
 (2010?浙江)已知:
(2010?浙江)已知:

 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: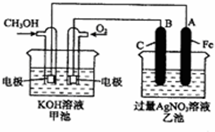 (2008?枣庄一模)如图是一个化学反应过程的示意图.已知甲池的总反应式为:
(2008?枣庄一模)如图是一个化学反应过程的示意图.已知甲池的总反应式为: