12.将1.28gCu投入一定量的浓HNO3溶液中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下的气体448mL,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的氧气,恰好使气体完全溶于水,则通入的氧气的体积为( )
| A. | 112 mL | B. | 224 mL | C. | 336 mL | D. | 448 mL |
7.铬酸钙(CaCrO4)俗称钙铬黄,溶于水.广泛用作氧化剂、腐蚀抑制剂、颜料等.铬铁矿中铬的含量为19.5%,其主要成分为 FeO•Cr2O3,还含Fe2O3、SiO2、Al2O3等杂质,以该铬铁矿为原料制备钙铬黄的工艺流程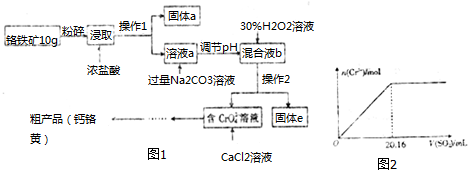
如图1已知:①过氧化氢能将Cr(OH)3氧化为CrO42-.
②金属离子氢氧化物开始沉淀时和沉淀完全时的pH及Ksp如下:
(1)将铬铁矿粉碎的目的是增大接触面积、提高浸取率.
(2)操作I的名称是过滤,固体a的主要成分是SiO2.
(3)写出浸取时生成Al3+的离子方程式:Al2O3+6H+=2Al3++3H2O.
(4)调节pH的范围是C.
A.3.5〜4.0 B.4.6〜5.4 C.5.9〜7.5
(5)写出H2O2氧化Cr(OH)3生成Na2CrO4的化学方程式2Cr(OH)3+3H2O2+2Na2CO3=2Na2CrO4+6H2O+2CO2↑.
(6)当溶液中Al3+开始沉淀时,c(Fe3+)=2.5×10-8mol/L.
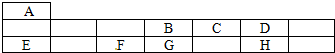
(7)取粗产品用硝酸酸化,再加水配制成1000mL溶液,取20mL于试管中,通入标准状况下SO2的体积与铬离子(Cr3+)物质的量的关系如图2该工艺流程中铬铁矿中铬的利用率是80%.[已知氧化性:CrO42->NO3 (H+)].

如图1已知:①过氧化氢能将Cr(OH)3氧化为CrO42-.
②金属离子氢氧化物开始沉淀时和沉淀完全时的pH及Ksp如下:
| 氢氧化物 | Ksp | 开始沉淀时的pH | 沉淀完全的pH |
| Fe(OH)3 | 2.5×10-38 | 2.3 | 3.5 |
| Fe(OH)2 | 1.0×10-15 | 7.5 | 9.5 |
| Al(OH)3 | 2.0×10-32 | 4.0 | 5.4 |
| Cr(OH)3 | 5.4×10-31 | 4.6 | 5.9 |
(2)操作I的名称是过滤,固体a的主要成分是SiO2.
(3)写出浸取时生成Al3+的离子方程式:Al2O3+6H+=2Al3++3H2O.
(4)调节pH的范围是C.
A.3.5〜4.0 B.4.6〜5.4 C.5.9〜7.5
(5)写出H2O2氧化Cr(OH)3生成Na2CrO4的化学方程式2Cr(OH)3+3H2O2+2Na2CO3=2Na2CrO4+6H2O+2CO2↑.
(6)当溶液中Al3+开始沉淀时,c(Fe3+)=2.5×10-8mol/L.
(7)取粗产品用硝酸酸化,再加水配制成1000mL溶液,取20mL于试管中,通入标准状况下SO2的体积与铬离子(Cr3+)物质的量的关系如图2该工艺流程中铬铁矿中铬的利用率是80%.[已知氧化性:CrO42->NO3 (H+)].
6.X、Y、Z、W为原子序数依次增大的短周斯元素,相关信息如图所示.下列判断正确的是( )

| A. | 原子半径:r(W)>r(Z)>r(Y) | |
| B. | 含Y元素的盐溶液一定显酸性 | |
| C. | 最高价氧化物对应水化物的酸性:Z>W | |
| D. | X、W分别形成的简单气态氢化物可反应生成离子化合物 |
5.用标准浓度的NaOH溶液来滴定未知浓度的盐酸,在下列操作中,会使盐酸测定浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,就加待测液
③滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
④滴定后俯视滴定管读数读取NaOH溶液的体积.
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,就加待测液
③滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
④滴定后俯视滴定管读数读取NaOH溶液的体积.
| A. | ②③ | B. | ①③ | C. | ①④ | D. | ③④ |
4.通过以下反应均可获取H2.下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H2=+206.1kJ•mol-1
③焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ•mol-1 .
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g)△H1=+571.6kJ•mol-1
②甲烷与水反应制氢:CH4(g)+H2O(g)=CO(g)+3H2(g)△H2=+206.1kJ•mol-1
③焦炭与水反应制氢:C(s)+H2O(g)=CO(g)+H2(g)△H3=+131.3kJ•mol-1 .
| A. | 反应①中电能转化为化学能 | |
| B. | 反应②使用催化剂,△H2减小 | |
| C. | 反应③中反应物的总能量高于生成物的总能量 | |
| D. | 反应CH4(g)=C(s)+2H2(g)的△H=+74.8kJ•mol-1 |
3.CO(g)+H2O(g)═H2(g)+CO2(g)△H<0,在其他条件不变的情况下( )
0 159509 159517 159523 159527 159533 159535 159539 159545 159547 159553 159559 159563 159565 159569 159575 159577 159583 159587 159589 159593 159595 159599 159601 159603 159604 159605 159607 159608 159609 159611 159613 159617 159619 159623 159625 159629 159635 159637 159643 159647 159649 159653 159659 159665 159667 159673 159677 159679 159685 159689 159695 159703 203614
| A. | 加入催化剂,改变了反应的途径,反应的△H也随之改变 | |
| B. | 反应物总能量小于生成物总能量 | |
| C. | 若在原电池中进行,反应放出的热量不变 | |
| D. | 升高温度,反应速率加快,但反应的△H不变 |

 .
. 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.