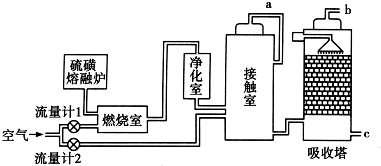
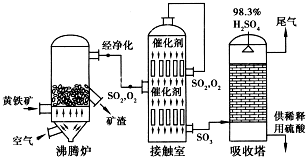
20.参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )

| A. | 该反应为可逆反应 | B. | 加入催化剂,可提高HBr的产率 | ||
| C. | 反应物总能量低于生成物总能量 | D. | 反应物总键能低于生成物总键能 |
19.下列物质,其水溶液能导电、溶于水时化学键被破坏,但物质本身属于非电解质的是( )
| A. | C12 | B. | NH3 | C. | BaCO3 | D. | C2H5OH (乙醇) |
17.CCTV《科技博览》曾经报道中科院首创用二氧化碳合成可降解塑料:聚二氧化碳.下列相关说法合理的是( )
| A. | 使用聚二氧化碳塑料会产生白色污染 | |
| B. | 聚二氧化碳塑料是通过聚合反应制得的 | |
| C. | 聚二氧化碳塑料与干冰互为同分异构体 | |
| D. | 聚二氧化碳塑干冰都属于纯净物 |
15.下列食品加工方法对人体无害的是 ( )
①用福尔马林浸泡海鲜防止鱼虾变质 ②香肠中加大量亚硝酸钠以保持肉类新鲜
③用“牛肉膏”将猪肉加工成牛肉 ④用“瘦肉精”(一种含激素的饲料)喂养生猪
⑤用小苏打做发酵粉制面包 ⑥向乳制品添加三聚氰胺以提高含氮量.
①用福尔马林浸泡海鲜防止鱼虾变质 ②香肠中加大量亚硝酸钠以保持肉类新鲜
③用“牛肉膏”将猪肉加工成牛肉 ④用“瘦肉精”(一种含激素的饲料)喂养生猪
⑤用小苏打做发酵粉制面包 ⑥向乳制品添加三聚氰胺以提高含氮量.
| A. | ②⑤ | B. | ⑤ | C. | ②③⑤ | D. | ①②③④⑤⑥ |
14.在工农业生产和日常生活中有很多化学问题.下列说法正确的是( )
0 159481 159489 159495 159499 159505 159507 159511 159517 159519 159525 159531 159535 159537 159541 159547 159549 159555 159559 159561 159565 159567 159571 159573 159575 159576 159577 159579 159580 159581 159583 159585 159589 159591 159595 159597 159601 159607 159609 159615 159619 159621 159625 159631 159637 159639 159645 159649 159651 159657 159661 159667 159675 203614
| A. | 明矾净水与液氯净水的原理相同 | |
| B. | 将草木灰和硫铵混合施用,肥效更高 | |
| C. | 冬季形成的大雾属于气溶胶 | |
| D. | 电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
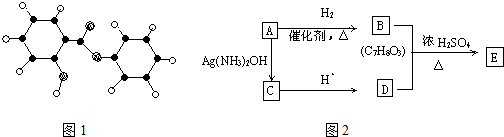

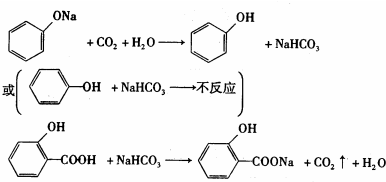 .
.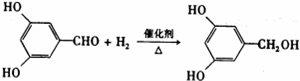 ;反应类型:加成反应.
;反应类型:加成反应.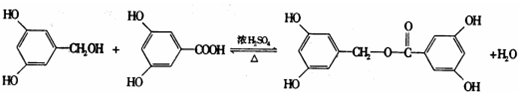 ;反应类型:酯化反应
;反应类型:酯化反应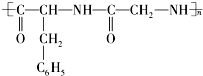 的单体是( )
的单体是( )