5.在c(Na+)为0.5mol•L-1的某溶液中,还可能含有下表中的若干离子.
取该溶液100mL进行如下实验(不考虑气体的溶解且气体体积是在标准状况下测定的).
试回答下列问题.
(1)由实验Ⅰ、Ⅱ可以得出的结论是原溶液中一定存在的离子有NH4+、CO32-、SO42-.
(2)实验Ⅱ中沉淀被溶解的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,Mg2+与CO32-不能大量共存的原因是Mg2++CO32-=MgCO3↓(用离子方程式表示).
(3)由实验Ⅲ得出原溶液中含有Cl-,你认为该观点是否正确?不正确(填“正确”或“不正确”),原因是步骤Ⅱ加入了氯离子.
(4)填写下表中各离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“×”)
(5)你认为原溶液中是否存在NO3-?不能确定(填“存在”、“不存在”或“不能确定”).原溶液中同时存在Cl-和NO3-,则c(NO3-)+c(Cl-)=0.4mol•L-1.
| 阳离子 | NH4+、Mg2+ |
| 阴离子 | Cl-、CO32-、SO42-、NO3- |
| 序号 | 实验内容 | 实验现象 |
| Ⅰ | 向该溶液中加入足量Ba(OH)2溶液并加热 | 产生6.27g白色沉淀并放出1.12L有刺激性气味的气体 |
| Ⅱ | 将Ⅰ得到的沉淀中滴加足量的稀盐酸 | 有气体放出,沉淀变为2.33g |
| Ⅲ | 向Ⅱ反应后的滤液中滴加AgNO3溶液 | 有白色沉淀产生 |
(1)由实验Ⅰ、Ⅱ可以得出的结论是原溶液中一定存在的离子有NH4+、CO32-、SO42-.
(2)实验Ⅱ中沉淀被溶解的离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,Mg2+与CO32-不能大量共存的原因是Mg2++CO32-=MgCO3↓(用离子方程式表示).
(3)由实验Ⅲ得出原溶液中含有Cl-,你认为该观点是否正确?不正确(填“正确”或“不正确”),原因是步骤Ⅱ加入了氯离子.
(4)填写下表中各离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“×”)
| 阴离子 | NH4+ | Mg2+ | CO32- | SO42- |
| c/mol•L-1 | 0.5mol/L | × | 0.2mol/L | 0.1mol/L |
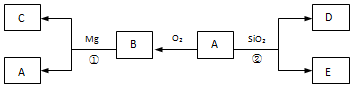
1.某混合物X由Na2O、Fe2O3、Cu、SiO2中的一种或几种物质组成.某兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是( )


| A. | 无法判断混合物中是否含有Na2O | B. | 由Ⅱ可知X中一定存在SiO2 | ||
| C. | 1.92g固体成分为Cu | D. | 15.6g混合物X中m(Fe2O3):m(Cu)=1:1 |
20.向含b mol Na2CO3的溶液中缓慢滴加含a mol HCl溶液,并不断振荡,下列说法不正确的是( )
| A. | 当$\frac{a}{b}$>2时,发生的离子反应为:CO32-+H+═HCO3-,HCO3-+H+═CO2↑+H2O | |
| B. | 当0<$\frac{a}{b}$<1时,发生的离子反应为:CO32-+H+═HCO3- | |
| C. | 当2a=3b时,发生的离子反应为:2CO32-+3H+═HCO3-+CO2↑+H2O | |
| D. | 当1<$\frac{a}{b}$<2时,溶液中n(HCO3-)为(2a-b)mol |
19.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | pH=1的H2SO4溶液,含H+的数目为2NA | |
| B. | 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| C. | 273K,101kPa下,14g乙烯与丙烯混合物中含有碳原子数目为3NA | |
| D. | 0.2mol C2H6O分子中一定存在0.2NA个碳碳单键 |
18.下列说法正确的是( )
0 159449 159457 159463 159467 159473 159475 159479 159485 159487 159493 159499 159503 159505 159509 159515 159517 159523 159527 159529 159533 159535 159539 159541 159543 159544 159545 159547 159548 159549 159551 159553 159557 159559 159563 159565 159569 159575 159577 159583 159587 159589 159593 159599 159605 159607 159613 159617 159619 159625 159629 159635 159643 203614
| A. | Mg3N2晶体中的化学键是共价键 | |
| B. | 某物质含有离子键,则该物质在任何条件下均能导电 | |
| C. | 干冰是分子晶体,其气化过程中只需克服分子间作用力 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
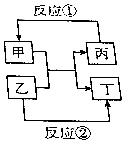 物质甲、乙、丙、丁的相互转化关系如图所反应所示(部分反应物、产物及反应条件已略去),已知甲为常见金属(Na、Mg、Al、Fe、Cu)或其氧化物.回答下列间题:
物质甲、乙、丙、丁的相互转化关系如图所反应所示(部分反应物、产物及反应条件已略去),已知甲为常见金属(Na、Mg、Al、Fe、Cu)或其氧化物.回答下列间题:
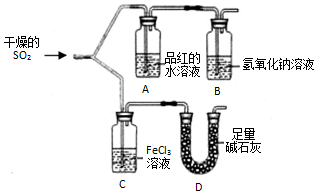 如图装置进行SO2气体性质实验.
如图装置进行SO2气体性质实验.