己知:KI溶液在酸性条件下能被空气中的O2氧化。
(1)写出发生反应的离子方程式_______________________。
(2)某化学小组为探究不同条件对上述反应速率的影响,设计如下实验,完成下表中①和②的内容。
(限选试剂:0.1 L mol/L硫酸、0.2 mol/L硫酸、1 mol/L KOH溶液、淀粉溶液)
组别 | 温度 | KI溶液 | H2SO4溶液 | 淀粉溶液 | 实验目的 | ||
c(KI) | Υ | c(H2SO4) | Υ | ||||
1 | 298K | 1 mol/L | 5 mL | 0.1mol/L | 5 mL | 3滴 | l组和2组探究②__________对该反应速率的影响;1组和3组探究反应物浓度对该反应速率的影响 |
2 | 308K | 1 mol/L | 5 mL | 0.1mol/L | 5 mL | 3滴 | |
3 | 298K | 1 mol/L | 5 mL | ①___________ | 5 mL | 3滴 | |
(3)在上述实验中,三种溶液混合的顺序最合理的是_______(选填下列选项);应记录的是_________所需的时间。
A.先将硫酸溶液与淀粉溶液混合,然后再加入KI溶液
B.先将KI溶液与硫酸溶液混合,然后再加 入淀粉溶液
入淀粉溶液
C.先将KI溶液与淀粉溶液混合,然后再加入硫酸溶液
KMnO4在实验室和工业生产中有广泛用途。
Ⅰ.某小组拟用酸性KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/L H2C2O4溶液、0.010 mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽。(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)
物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010 mol/L KMnO4溶液) | m(MnSO4固体)/g | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 0 | 50 | |
② | 2.0 | 0 | 4.0 | 0 | 25 | |
③ | 1.0 | a | 4.0 | 0 | 25 | |
④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
回答下列问题:
(1)完成上述反应原理的离子反应方程式_______________________。
(2)上述实验①②是探究____________对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则a为___________;乙是实验需要测量的物理量,则表格中“乙”应填写___________;上述实验②④是探究_________对化学反应速率的影响。

Ⅱ.某化学小组利用如图装置进行实验证明氧化性:KMnO4>Cl2>Br2。限选试剂:KBr溶液、KMnO4、浓盐酸、浓硫酸。
(3)装置d中观察到的现象为____________________;此实验装置的不足之处是无尾气吸收装置,请写出处理尾气的离子方程式_____________________。
氢、氧两种元素组成的常见物质有H2O和H2O2,二者在一定条件下均可分解。
(1)已知:
化学键 | 断开1mol化学键所需的能量(kJ) |
H-H | 436 |
O-H | 463 |
O=O | 498 |
①H2O的电子式是________________。
②H2O(g)分解的热化学方程式是________________________。
③11.2 L(标准状况)的H2完全燃烧,生成气态水,放出__________kJ的热量。
(2)某同学以H2O2分解为例,探究浓度与溶液酸碱性对反应速率的影响。常温下,按照如表所示的方案完成实验。
实验编号 | 反应物 | 催化剂 | |
a | 50 mL5%H2O2溶液 | 1 mL0.1 mol·L-1FeCl3溶液 | |
b | 50 mL5%H2O2溶液 | 少量浓盐酸 | 1 mL0.1 mol·L-1FeCl3溶液 |
c | 50 mL5%H2O2溶液 | 少量浓NaOH溶液 | 1 mL 0.1 mol·L-1FeCl3溶液 |
d | 50 mL5%H2O2溶液 | MnO2 | |
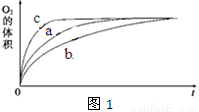
① 测得实验a、b、c中生成氧气的体积随时间变化的关系如图1所示。由该图能够得出的实验结论是______________________。
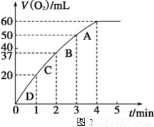
② 测得实验d在标准状况下放出氧气的体积随时间变化的关系如图2所示。解释反应速率变化的原因________________;计算H2O2的初始物质的量浓度为________________ (保留两位有效数字)。
 /mL
/mL 有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。

 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。请回答下列问题:
