硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程图如下:

(1)将菱锌矿研磨成粉的目的是_____。
(2)完成“氧化除铁”步骤中反应的离子方程式:□Fe(OH)2+□____+□_____=□Fe(OH)3+□CI-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,摩尔质量为89g/mol,化学式是_______。以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时针铁矿转化为Fe(OH)2,该电池放电反应的化学方程式是__________。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
沉淀化学式 | Mg(OH)2 | Zn(OH)2 | MgCO3 | CaCO3 |
开始沉淀的pH | 10.4 | 6.4 | — | — |
沉淀完全的pH | 12.4 | 8.0 | — | — |
开始溶解的pH | — | 10.5 | — | — |
Ksp | 5.6× | — | 6.8× | 2.8× |
(5)工业上从“滤液3”制取MgO过程中,合适的反应物是______(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.氨水
(6)“滤液4”之后的操作依次为______、_______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于________(用代数式表示)
下列有关实验现象和解释或结论都正确的选项是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 将电石与水反应产生的气体通入酸性高锰酸钾溶液 | 紫色褪去 | 证明有乙炔生成 |
B | 将滴有酚酞的碳酸钠溶液加热 | 红色变深 | 水解过程是吸热的 |
C | 把Cl2通入紫色石蕊试液中 | 紫色褪去 | Cl2具有漂白性 |
D | 向碳酸钙粉末中滴加稀盐酸 | 有气泡产生 | 非金属性氯强于碳 |

 CH3OH(g)△H1=—99kJ.mol-1,
CH3OH(g)△H1=—99kJ.mol-1,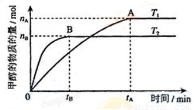





 的盐酸和硫酸反应,后者更剧烈
的盐酸和硫酸反应,后者更剧烈 。下列说法正确的是
。下列说法正确的是


