由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次发生的反应类型和反应条件都正确的是( )
选项 | 反应类型 | 反应条件 |
A | 加成反应、取代反应、消去反应 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
B | 消去反应、加成反应、取代反应 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
C | 氧化反应、取代反应、消去反应 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
D | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
第1小题:下表所示的是关于有机物A、B的信息:
A | B |
①能使溴的四氯化碳溶液褪色 | ①由C、H两种元素组成 |
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的产物的名称为______________。
(2) B具有的性质是________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤能使酸性KMnO4溶液和溴水褪色 ⑥任何条件下均不与氢气反应 ⑦与溴水混合后液体分层且上层呈橙红色
(3) A的同系物用通式CnHm表示,B的同系物用通式CxHy表示,当CnHm、CxHy分别出现同分异构体时,碳原子数的最小值n=________,x=________。
第2小题:有如下图所示某有机物,根据该有机物的结构回答:
①该物质中的含氧官能团有________、________(写名称,下同),此外还含有的官能团是________。
②该物质既可以与溴水发生________反应和________反应,也可以与酸性KMnO4溶液因发生______反应而使其褪色,当遇到FeCl3溶液时发生显色反应而呈________色。
③若1 mol该物质与足量H2反应,消耗H2的物质的量为________,若与足量溴水反应,消耗Br2的物质的量为________,若与足量氢氧化钠溶液反应,消耗NaOH的物质的量为________。
 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )

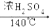 CH3CH2—O—CH2CH3 (乙醚)+H2O
CH3CH2—O—CH2CH3 (乙醚)+H2O






 为原料制备
为原料制备 的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂作用)。合成路线流程图示例如下:

 出又有气体逸出的是
出又有气体逸出的是