0 148574 148582 148588 148592 148598 148600 148604 148610 148612 148618 148624 148628 148630 148634 148640 148642 148648 148652 148654 148658 148660 148664 148666 148668 148669 148670 148672 148673 148674 148676 148678 148682 148684 148688 148690 148694 148700 148702 148708 148712 148714 148718 148724 148730 148732 148738 148742 148744 148750 148754 148760 148768 203614


 2H++A2-
2H++A2-
 Cr2O72-
Cr2O72- ,已知废水中Cr的含量为26.0g·L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全。常温下
,已知废水中Cr的含量为26.0g·L-1,当溶液中离子浓度小于10-5mol/L时认为离子已经沉淀完全。常温下 。有关叙述中不正确的是
。有关叙述中不正确的是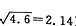 )。
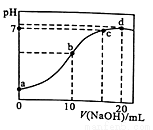
)。
 CH3OCH3(g)+H2O(g) △H=-204.7kJ/mol。
CH3OCH3(g)+H2O(g) △H=-204.7kJ/mol。