(14分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
分组实验 | 催化剂 | |
① | 10mL 5% H2O2溶液 | 无 |
② | 10mL 2% H2O2溶液 | 无 |
③ | 10mL 5% H2O2溶液 | 1mL 0.1mol•L﹣1FeCl3溶液 |
④ | 10mL 5%H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L﹣1FeCl3溶液 |
⑤ | 10mL 5% H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L﹣1FeCl3溶液 |
(1)写出实验③中H2O2分解反应方程式并标明电子转移的方向和数目: .
(2)实验①和②的目的是 .
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是 .
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图1.分析上图能够得出的实验结论: 环境能增大H2O2分解的速率; 环境能减小H2O2分解速率.
(4)将0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图2所示.解释反应速率变化的原因: ,计算H2O2的初始物质的量浓度为 .(保留两位有效数字,在标准状况下测定)

下列实验操作正确的是
选项 | 实验 | 操作 |
A | 验证氯气和溴的非金属性强弱 | 将少量氯水加入盛有溴化亚铁溶液的试管中,用力振荡后加入少量乙醇,振荡,静置。 |
B | 检验溶液中是否含有SO42- | 用HNO3溶液酸化后再加氯化钡溶液 |
C | 证明浓硫酸有脱水性和强氧化性 | 将浓硫酸滴到蔗糖表面 |
D | 制取氢氧化铁胶体 | 将烧碱溶液滴加到氯化铁溶液中 |


 N2 (g)+CO2 (g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是
N2 (g)+CO2 (g)△H=-373.2KJ/mol,达到平衡后,为提高NO的转化率和该反应的速率,可采取的措施是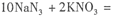
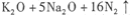 。下列判断正确的是
。下列判断正确的是