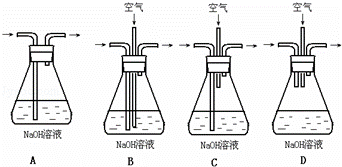
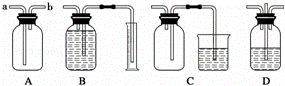
取一定量的铁、铜混合物粉末,平均分成五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(稀硝酸的唯一还原产物)的体积及所得剩余固体的质量记录如下(所有气体的体积均在标况下测定)
| 实验序号 | 1 | 2 | 3 | 4 | 5 |
| HNO3溶液的体积(mL) | 100 | 200 | 300 | 400 | 500 |
| 剩余固体质量(g) | 17.2 | 8 | 0 | 0 | 0 |
| 气体体积(L) | 2.24 | 4.48 | 6.72 | 7.84 | 7.84 |
(1)该实验中所用硝酸的物质的量浓度
(2)第一次实验后剩余固体为 ,第二次实验剩余固体为 (均填写化学式)
(3)求实验中每次所取混合物中铜的质量 .
在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如表所示:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为 mol•L﹣1•s﹣1.
(2)n3 n4(填“>”、“<”或“=”),该反应的平衡常数为 (保留小数点后一位).
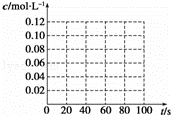
(3)若在相同情况下,最初向该容器中充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是 mol•L﹣1,假设在80s时达到平衡,请在如图中画出并标明该条件下此反应中N2O4和NO2的浓度随时间变化的曲线.
(4)达到平衡后,如升高温度,气体颜色会变深,则升高温度后,反应2NO2(g)⇌Ν2O4(g)的平衡常数将 (填“增大”、“减小”或“不变”).
(5)达到平衡后,如向该密闭容器中再充入0.32mol氦气,并把容器体积扩大为4L,则平衡将 (填“向左移动”、“向右移动”或“不移动”).
下列关于实验的说法错误的是( )
|
| A. | “硝基苯制备”实验中,将温度计插入水浴,但水银球不能与烧杯底部和烧杯壁接触 |
|
| B. | 除去干燥CO2中混有的少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
|
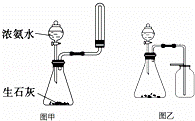
| C. | 选择合适的试剂,用图乙所示装置可分别制取并收集少量CO2和O2 |
|
| D. | 实验室用图甲所示的装置制取少量氨气 |

 (其中:﹣X、﹣Y均为官能团).
(其中:﹣X、﹣Y均为官能团).