下表对某些反应方程式的评价合理的是
编号 | 离子方程式或电极反应式 | 评价 | |
A | 次氯酸钙溶液中通入足量SO2 | Ca2++C1O-+SO2+H2O=CaSO4+ C1-+2H+ | 正确 |
B | 硫酸铁溶液与氢氧化钡溶液混合 | Fe3++SO42-+Ba2++3OH- = Fe(OH)3↓+BaSO4↓ | 正确 |
C | 醋酸铵溶于水 | CH3COO—+NH4+ | 错误,阴离子水解相互促进,应该用“=”号 |
D | 用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 | 阴极:2Cu2++4e-= 2Cu 阳极:4OH--4e-= 2H2O+O2↑ | 错误,该阴阳两极反应不可能同时发生 |

 CO2+H2①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的
CO2+H2①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的
 所用试剂是_______________________。
所用试剂是_______________________。

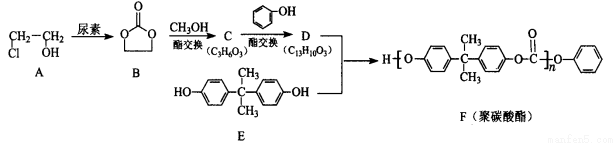

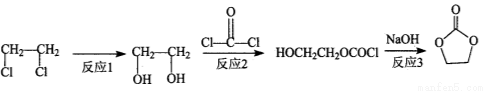
 )结构
)结构 CH3COOH++NH3·H2O
CH3COOH++NH3·H2O
