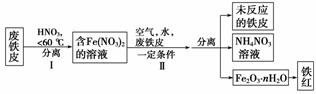
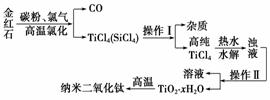
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。工业上以金红石(主要成分是TiO2,主要杂质是SiO2)制取纳米级二氧化钛的流程如下:
| 资料卡片 | ||
| 物质 | 熔点 | 沸点 |
| SiCl4 | -70 ℃ | 57.6 ℃ |
| TiCl4 | -25 ℃ | 136.5 ℃ |
(1)写出氯化时生成TiCl4的化学方程式________________________。
(2)操作Ⅰ、操作Ⅱ名称分别是____________________、____________。
(3)写出TiCl4水解的化学方程式________________。
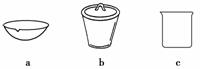
(4)如在实验室中完成灼烧TiO2·xH2O放在________(填字母序号)中加热。
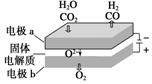
(5)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2。H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的________(填“氧化性”或“还原性”)。
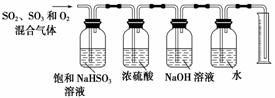
(6)某研究小组用下列装置模拟“生态马路”的部分原理并测定CO的转化效率(夹持装置已略去)。
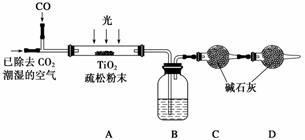
①B装置中的药品名称为________,若通入2.24 L(已折算成标准状况)CO气体和足量空气,最终测得装置A增重1.1 g,则CO的转化率为________。
②实验①中,当CO气体全部通入后,还要再通一会儿空气,其目的是____________。
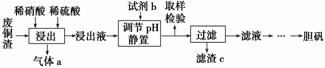
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
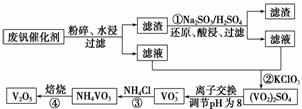
部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式________________。
(2)图中所示滤液中含钒的主要成分为____________(写化学式)。
(3)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为 VO
VO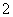 +
+ H2C2O4+
H2C2O4+ ________===
________=== VO2++
VO2++ CO2↑+
CO2↑+ H2O。
H2O。
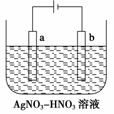
(4)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO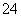 。电池放电时,负极的电极反应为V2+-e-===V3+。
。电池放电时,负极的电极反应为V2+-e-===V3+。
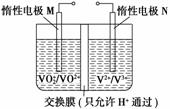
①电池放电时的总反应方程式为__________________。充电时,电极M应接电源的________极;
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+。则第一步反应过程中阴极区溶液n(H+)________(填“增大”、“不变”或“减小”),阳极的电极反应式为______________。
X、Y、Z是三种常见的单质,甲、乙是两种常见的化合物。下表各组物质之间通过一步反应不能实现如图所示转化的是( )
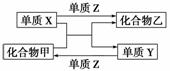
| 选项 | X | Y | Z | 甲 | 乙 |
| A | H2 | Si | Cl2 | SiCl4 | HCl |
| B | Mg | C | O2 | CO2 | MgO |
| C | Zn | Fe | Cl2 | FeCl2 | ZnCl2 |
| D | Cl2 | N2 | H2 | NH3 | HCl |
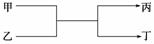
X、Y、Z、W四种物质的转化关系如图所示。下列组合中不符合转化关系的是( )
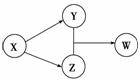
| 选项 | X | Y | Z | W |
| A | 浓盐酸 | FeCl2 | Cl2 | FeCl3 |
| B | Na2O2 | NaOH | Na2CO3 | NaHCO3 |
| C | Na2CO3 | CO2 | CaCO3 | Ca(HCO3)2 |
| D | SO2 | Na2SO3 | H2SO4 | NaHSO3 |
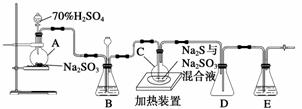
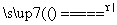 Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)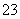 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O