海水中不仅含有丰富 的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
的非金属元素资源(如氯、溴、碘等),还含有丰富的金属元素资源(如Na、Mg、Fe、Cr等)。
(1)海水晒盐的原理是:________;写出氯化钠的电子式:________;与Na、Cl同周期,且简单离子半径最小的离子结构示意图:________。
(2)晒出的粗盐常混有MgSO4、CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,②________,③加过量Na2CO3溶液,④________,⑤过滤除去杂质,⑥________,⑦蒸发结晶。
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+、Cr3+等,为富集镁使其转化为MgCl2晶体,必须除去这些杂质离子。
有关资料:
| M(OH) | pH | |
| 开始沉淀 | 沉淀完全 | |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mg(OH)2 | 9.5 | 11.0 |
| Cr(OH)3 | 4.3 | 5.0 |
为了有效除去杂质离子,又不引入新的杂 质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加________,目的是________;
②再加________,目的是________;
③过滤后,为能得到纯净的MgCl2晶体,采用的操作方法是:
_______________ __________________________________
__________________________________
__________________________________________________。
所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物。根据下列四种金属的熔、沸点,判断其中不能形成合金的是( )
| Na | Cu | Al | Fe | |
| 熔点/℃ | 97.5 | 1083 | 660 | 1535 |
| 沸点/℃ | 883 | 2595 | 2200 | 3000 |
A. Cu和Al B. Fe和Cu
C. Fe和Na D. Al和Na

 ______________________;
______________________;
 r2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是( )
r2===2Fe3++2Br-,2Fe3++2I-===2Fe2++I2。则下列有关说法中,不正确的是( )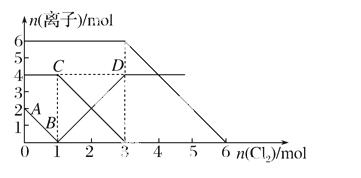
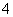 的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH
的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示,则原溶液中Al3+、Mg2+、NH
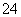 )=0.5 mol·L-1
)=0.5 mol·L-1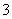 )=0.08 mol
)=0.08 mol 等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是( )
等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是( )
 ,则与过量NH3·H2O也生成AlO
,则与过量NH3·H2O也生成AlO