0 142798 142806 142812 142816 142822 142824 142828 142834 142836 142842 142848 142852 142854 142858 142864 142866 142872 142876 142878 142882 142884 142888 142890 142892 142893 142894 142896 142897 142898 142900 142902 142906 142908 142912 142914 142918 142924 142926 142932 142936 142938 142942 142948 142954 142956 142962 142966 142968 142974 142978 142984 142992 203614
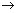 Se+I2+KNO3十H2O
Se+I2+KNO3十H2O L-1的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为
L-1的Na2S2O3溶液25.00mL,所测定的样品中SeO2的质量分数为 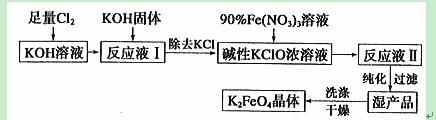
 KCl+KClO+H2O(条件:温度较低)
KCl+KClO+H2O(条件:温度较低)

