一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
| t / min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2) / mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6 min的平均反应速率:
B.6~10 min的平均反应速率:
C.反应至6 min时,

D.反应至6 min时,H2O2分解了50%
某温度下,H2(g)+CO2(g) H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
H2O(g)+CO(g)的平衡常数K=2.25。该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示。
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A.反应开始时,反应速率:甲<乙<丙
B.平衡时,甲中和丙中H2的转化率均是
 60%
60%
C.平衡时,c(CO2)丙=2c(CO2)甲
D.平衡时,乙中CO2的体积分数大于60%
在一容积不变的密闭容器中通入A、B两种气体,一定条件下发生如下反应:
2A(g)+B(g) 2C(g);△H<0
2C(g);△H<0
达到平衡后,只改变一个条件(x),下列量(y)的变化一定符合图中曲线的是
| x | y | |
| A | 再加入A | B的转化率 |
| B | 再加入C | A的体积分数 |
| C | 增大体积 | A的转化率 |
| D | 降低温度 | 混合气体的密度 |

 N2O4(g) △H= -57 kJ·mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
N2O4(g) △H= -57 kJ·mol-1,在条件下温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
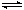 cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是
cC(g)+d D(g),当其他条件不变时,反应过程中某物质在混合物中的百分含量与温度(T)、压强(P)的关系如图所示,下列判断正确的是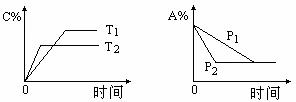
 2AB3(g)△H >0下列图象中正确的是
2AB3(g)△H >0下列图象中正确的是 
 HBr+HBrO,当加入NaOH溶液后颜色变浅
HBr+HBrO,当加入NaOH溶液后颜色变浅 W+Z,反应速率(V)随时间(t)变化的
W+Z,反应速率(V)随时间(t)变化的 情况如图所示。
情况如图所示。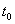 表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是
表示在其他条件不变的情况下,改变体系的一个条件(温度、浓度、压强)所引起的变化。则下列分析正确的是