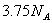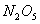 是一种新型硝化剂,在一定温度下可发生以下反应:
是一种新型硝化剂,在一定温度下可发生以下反应:
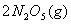

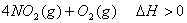
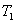 温度时,向密闭容器中通入
温度时,向密闭容器中通入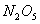 ,部分实验数据见下表:
,部分实验数据见下表:
|
| 0 | 500 | 1000 | 1500 |
|
| 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是( )
A. 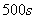 内
内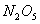 分解速率为
分解速率为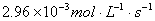
B. 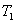 温度下的平衡常数
温度下的平衡常数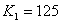 ,平衡时
,平衡时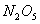 的转化率为50%
的转化率为50%
C. 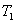 温度下的平衡常数为
温度下的平衡常数为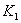 ,
,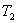 温度下的平衡常数为
温度下的平衡常数为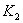 ,若
,若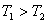 ,则
,则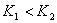
D. 达平衡后其他条件不变,将容器的体积压缩到原来的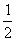 ,则再次平衡时
,则再次平衡时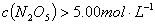
利用表中实验器材(规格和数量不限),能完成相应实验的一项是( )
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和苯除去 |
| B | 烧杯、玻璃棒、胶头滴管、滤纸 | 用盐酸除去硫酸钡中的少量碳酸钡 |
| C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体碳酸钠配制 |
| D | 烧杯、玻璃棒、胶头滴管、酒精灯 | 硫酸铜溶液的浓缩结晶 |
利用催化氧化反应将SO2转化为SO3是工业上生产
硫酸的关键步骤.
 (1)T1℃时,在1L密闭容器中充入0.6molSO3,图1表示SO3
(1)T1℃时,在1L密闭容器中充入0.6molSO3,图1表示SO3
物质的量随时间的变化曲线。
①平衡时,SO3的转化率为 (保留小数点后一位) ;
T1℃时,反应2SO2(g)+O2(g)  2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3)的变化曲线为 (填字母)。
2SO3(g) 的平衡常数为 ;其他条件不变,在8min时压缩容器体积至0.5L,则n(SO3)的变化曲线为 (填字母)。
②下表为不同温度(T)下,反应2SO2(g)+O2(g)  2SO3(g) (△H<0)的化学平衡常数(K)
2SO3(g) (△H<0)的化学平衡常数(K)
| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
由此推知,温度最低的是 (填“T1”、“T2” 或 “T3”)。
③在温度为T1℃时,向该1L的密闭容器中同时加入0.2molSO2、xmolO2、0.2molSO3三种气体,在达到平衡前若要使SO3的浓度减小,则x的取值范围是 。
 (2)科学家研究出用电化学原理生产硫酸的新工艺,装置如图2所示,总反应的化学方程式为 ,其阳极的电极反应式为
(2)科学家研究出用电化学原理生产硫酸的新工艺,装置如图2所示,总反应的化学方程式为 ,其阳极的电极反应式为
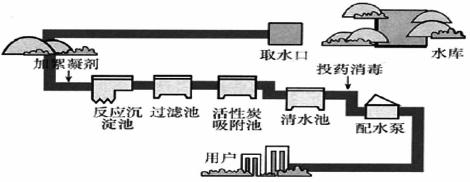
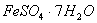 是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。
是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。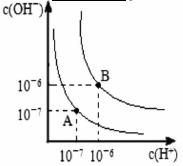
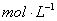 的NaOH溶液中,由水电离出的c(H+)=________
的NaOH溶液中,由水电离出的c(H+)=________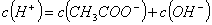
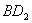 分子的电子式为__________,
分子的电子式为__________,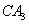 分子的空间立体构型为__________。
分子的空间立体构型为__________。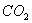 和液态
和液态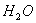 ,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。
,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________。某燃料电池用H作燃料,KOH为电解液,该电池的负极电极反应式为:________________________________________。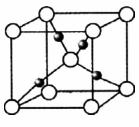


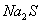 和
和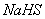 混合溶液中:
混合溶液中: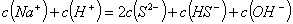
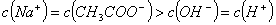
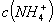 相等的①
相等的①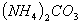 、②
、②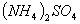 、③
、③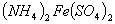 三种溶液中,溶质的物质的量浓度大小:①>②>③
三种溶液中,溶质的物质的量浓度大小:①>②>③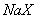 和弱酸
和弱酸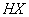 混合后呈酸性的溶液中:
混合后呈酸性的溶液中: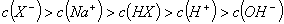
 溶液中少量
溶液中少量
 的溶液
的溶液 溶液与
溶液与 的反应:
的反应:

 氧化酸性溶液中的
氧化酸性溶液中的

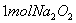 固体中含离子总数为
固体中含离子总数为
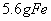 与足量稀
与足量稀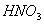 反应,转移
反应,转移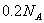 个电子
个电子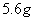 乙烯与丁烯的混合物中含有的氢原子的数目为
乙烯与丁烯的混合物中含有的氢原子的数目为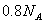
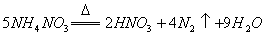 反应中,生成
反应中,生成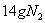 时,转移的电子数目为
时,转移的电子数目为