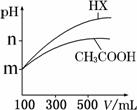
100mL 浓度为2mol•L﹣1的盐酸跟过量的锌片反应,为加快反应速率,又基本不影响生成氢气的总量,可采用的方法是( )
|
| A. | 加入适量的6mol•L﹣1的盐酸 | B. | 加入数滴氯化铜溶液 |
|
| C. | 加入适量蒸馏水 | D. | 加入适量的氯化钠溶液 |
燃料电池是燃料(如CO、H2、CH4等)跟O2(或空气)反应,将化学能转化为电能的装置,电解质溶液是强碱溶液.下列关于CH4燃料电池的说法正确的是( )
|
| A. | 放电时溶液中的阴离子向正极移动 |
|
| B. | 负极反应式为:CH4+10OH﹣﹣8e﹣=CO32﹣+7H2O |
|
| C. | 随着放电的进行,溶液的pH不变 |
|
| D. | 负极反应式为:O2+2H2O+4e=4OH﹣ |
一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)⇌H2(g)+I2(g).若c(HI)由0.1mol/L 降到0.07mol/L时,需要15s,那么c(HI)由0.07mol/L 降到0.05mol/L时,所需反应的时间为( )
|
| A. | 等于5 s | B. | 等于10 s | C. | 大于10 s | D. | 小于10 s |
下列说法不正确的是( )
|
| A. | 金属腐蚀就是金属原子失去电子被氧化的过程 |
|
| B. | 钢铁吸氧腐蚀时,正极反应式为:2H2O+O2+4e﹣=4OH﹣ |
|
| C. | 氯碱工业中,阳极发生的反应为:2Cl﹣﹣2e﹣=Cl2↑ |
|
| D. | 镀锌铁皮的镀层损坏后,铁更容易腐蚀 |
化学与生活、社会密切相关.下列说法不正确的是( )
|
| A. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
|
| B. | 提倡人们购物时不用塑料袋,是为了防止白色污染 |
|
| C. | 为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
|
| D. | 凡含有食品添加剂的食物对人体健康均有害,不可食用 |
下列说法不正确的是( )
|
| A. | 需要加热才能发生的化学反应不一定是吸热反应 |
|
| B. | 放热反应在常温下一定很容易发生 |
|
| C. | 在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓值差即焓变(△H)决定 |
|
| D. | 化学反应除了生成新的物质外,还伴随着能量的变化 |
化学理论在元素单质及其化合物反应中应用广泛。
(1)在一定条件下,可逆反应mA nB+pC ⊿H,达到平衡状态。
nB+pC ⊿H,达到平衡状态。
①若A、B、C都是气体,增大压强,平衡向逆反应方向移动,则m (填“大于”、“小于”或“等于”)n+p。
②其他条件不变,加热后A的质量增加,则反应⊿H________0(填“大于”、“小于”或“等于”)。
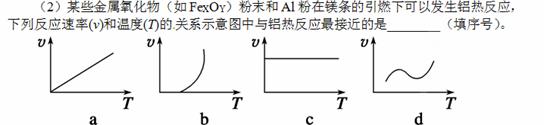 (3)一定温度下,发生反应:FeO(s)+CO(g)
(3)一定温度下,发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH。已知该反应在不同温度下的平衡常数如下表:
Fe(s)+CO2(g) ΔH。已知该反应在不同温度下的平衡常数如下表:
| 温度/℃ | 1000 | 1100 |
| 平衡常数 | 0.68 | 0.50 |
请回答下列问题:
①该反应的ΔH___ 0(填“>”、“<”或“=”)。
②T℃时,将FeO(s)和CO(g)各3.0 mol加入10 L的密闭容器中,反应达到平衡后,测得CO转化率为W1,c(CO2) =0.15mol·L-1,则温度T (填“高于”、“低于”、“等于”)1000, 若此时保持其它条件不变再充入2.0 mol CO(g),再达平衡时测得CO转化率为W2,则W1 (填“>”、“<”或“=”)W2。
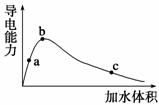
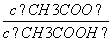 的比值 (填“增大”、“减小”、“等于”)。
的比值 (填“增大”、“减小”、“等于”)。