0 14137 14145 14151 14155 14161 14163 14167 14173 14175 14181 14187 14191 14193 14197 14203 14205 14211 14215 14217 14221 14223 14227 14229 14231 14232 14233 14235 14236 14237 14239 14241 14245 14247 14251 14253 14257 14263 14265 14271 14275 14277 14281 14287 14293 14295 14301 14305 14307 14313 14317 14323 14331 203614


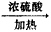 CO↑+CO2↑+H2O,下列装置中,可用作草酸分解制取气体的是_________。(填字母)
CO↑+CO2↑+H2O,下列装置中,可用作草酸分解制取气体的是_________。(填字母) 










