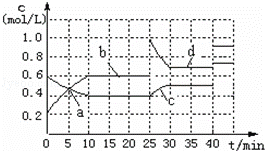
已知:2M(g)⇌ N(g);△H<0.现将M和N的混和
气体通入体积为1L的恒温密闭容器中,反应体系中各物质
的浓度随时间变化关系如图所示.下列说法正确的是:
|
| A. | a、b、c、d四个点中处于平衡状态的点是a、b |
|
| B. | 反应进行至25min时,曲线发生变化的原因是加入了 0.4mol N |
|
| C. | 若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
|
| D. | 若40min后出现如图所示变化,则可能是加入了某种催化剂 |
 2NH3的能量变化如右图所示,该反应的热化学方程式是:
2NH3的能量变化如右图所示,该反应的热化学方程式是:  2NH3(l) ΔH=2(a-b-c) kJ·mol-1
2NH3(l) ΔH=2(a-b-c) kJ·mol-1 N2(g)+
N2(g)+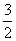 H2(g)
H2(g) 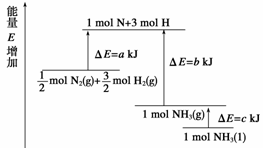
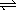 2Z(气)一定达到化学平衡状态的是:
2Z(气)一定达到化学平衡状态的是: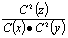 为一常数
为一常数 pC十qD,用A物质表示的平均反应速率为
pC十qD,用A物质表示的平均反应速率为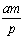 摩/(升·分),则t分钟时,D物质增加的物质的量是:
摩/(升·分),则t分钟时,D物质增加的物质的量是: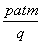 摩 B.
摩 B.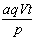 摩 C.
摩 C.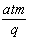 摩 D.
摩 D.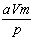 摩
摩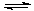 H++ SO42-用铂电极电解硫酸氢钾溶液,在阳极上生成S2O82-,S2O82-水解可以得到H2O2。写出阳极上的电极反应式 。
H++ SO42-用铂电极电解硫酸氢钾溶液,在阳极上生成S2O82-,S2O82-水解可以得到H2O2。写出阳极上的电极反应式 。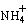 的废水会发生如下反应:
的废水会发生如下反应: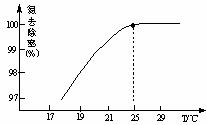 ①温度对氮处理率的影响如图所示。在25℃前,升高温度氮去除率增大的原因是 。
①温度对氮处理率的影响如图所示。在25℃前,升高温度氮去除率增大的原因是 。