0 141655 141663 141669 141673 141679 141681 141685 141691 141693 141699 141705 141709 141711 141715 141721 141723 141729 141733 141735 141739 141741 141745 141747 141749 141750 141751 141753 141754 141755 141757 141759 141763 141765 141769 141771 141775 141781 141783 141789 141793 141795 141799 141805 141811 141813 141819 141823 141825 141831 141835 141841 141849 203614


 离子的立体构型为________;
离子的立体构型为________;
 溶于水
溶于水

 的空间构型是________ (用文字描述)。
的空间构型是________ (用文字描述)。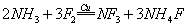

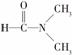
 )具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子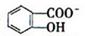 能形成分子内氢键。据此判断,相同
能形成分子内氢键。据此判断,相同 温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。 元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
 ①在1个晶胞中,X离子的数目为 。
①在1个晶胞中,X离子的数目为 。

 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为 。Si与O的原子数之比为 化学式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为 。Si与O的原子数之比为 化学式为 