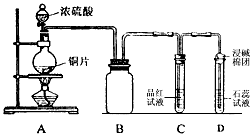
某化学小组采用类似制乙酸乙酯的装置(如下图),以环己醇制备环己烯



| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品:将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是 ▲ ,导管B除了导气外还具有的作用是 ▲ 。
②试管C置于冰水浴中的目的是 ▲ 。
(2)制备精品:
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在 ▲ 层(填上或下),分液后,用 ▲ (填编号)洗涤环己烯。
 A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液 D.NaOH溶液
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液 D.NaOH溶液
②再将环己烯按右图装置蒸馏,冷却水从 ▲ (填f或g)口进入,蒸馏时要加入生石灰,目的是 ▲ 。
③收集产品时,控制的温度应在 ▲ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是 ▲ 。
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,最简单的方法是 ▲ 。
A.酸性KMnO4溶液 B.用金属钠 C.测定沸点 D.溴的四氯化碳溶液
现有部分元素的性质与原子(或分子)结构如下表:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小 |
(1)写出元素T在元素周期表中的位置 ▲ 。
(2)元素Y与元素Z相比,金属性较强的是 ▲ (用元素符号表示),下列表述中能证明这一事实的是 ▲ (填序号)。
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
e.Y失去电子的数目比Z少
(3)T、X、Y、Z中有两种元素能形成一种淡黄色的固体,写出该化合物的电子式 ▲ ,该物质中含有的化学键是 ▲ 。
(4)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素形成的化合物W气态时密度等于氧气,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式 ▲ 。
(5) X与Z形成的化合物ZX结构类似金刚石,最高可稳定到2200℃,推测属于 ▲
晶体。打开盛有ZX的袋口可闻到氨气味,故应避水保存,写出变质反应的化学方程式
▲ 。
下列各组物质中,不管它们以何种比例混合,只要总物质的量一定,充分燃烧后消耗氧气的量一定的是
A.C2H2和C6H6 B.C2H6O和C3H6O2 C.CH2O和C2H4O2 D.C3H8和C4H8O2


 (X代表卤素)
(X代表卤素)
 ⑧
⑧
 。下列有关苹果酸的说法不正确的是
。下列有关苹果酸的说法不正确的是