化学与生活是紧密相连的,下列说法正确的是( )
| A、“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| B、海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 |
| C、生铁在潮湿的空气中易生锈,其负极反应式为:2H2O+O2+4e-=4OH- |
| D、BaSO4在医学上用做钡餐,Ba2+对人体无毒 |
下列离子方程式正确的是( )
| A、SiO2与NaOH溶液:SiO2+2Na++2OH-═Na2SiO3↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-═SO32-+2HClO |
| C、向含有0.4mol FeBr2的溶液中通入0.1mol Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
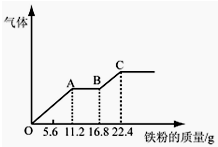 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A、原混合酸中NO3-物质的量浓度为2mol/L |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为2.5mol?L-1 |
X、Y、Z、W是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Z元素形成的单质,已知,它们可以发生如下反应:甲+乙→丁+己,甲+丙→戊+己;0.1mol/L丁溶液的pH为13(25℃).它们满足如图转化关系,下列说法正确的是( )
| A、Z元素在周期表中的位置为二周期第ⅥA族 |
| B、原子半径:W>Z>Y>X |
| C、1mol甲与足量的乙完全反应共转移了2mol电子 |
| D、1L 0.1mol/L戊溶液中阴离子总的物质的量小于0.1mol |
下列有关实验的操作正确的是( )
| A、实验时手掌不小心沾上苯酚,应立即用65℃以上的热水清洗防腐蚀 |
| B、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| C、实验室可以用浓硫酸与氯化钠固体共热制取氯化氢气体,因此浓硫酸与碘化钠固体共热也能制取碘化氢气体 |
| D、用化学方法检验甘油和酒精:可用新制的Cu(OH)2悬浊液 |
中学化学常见物质甲、乙、丙、丁之间存在转化关系:甲十乙→丙十丁.下列说法正确的是( )
| A、若甲为钠单质,丁为氢气,则乙一定是水 |
| B、若甲为铝单质,丁为铁单质,则乙一定是氧化铁 |
| C、若甲为铜单质,丁为氯化亚铁溶液,则乙一定是氯化铁溶液 |
| D、若甲、乙、丙、丁均为化合物,则该反应一定属于复分解反应 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明的溶液中:Na+、K+、MnO4-、AlO2- | ||
| B、0.1mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | ||
C、
| ||
| D、c(S2-)=0.1mol?L-1的溶液中:Na+、NH4+、ClO-、SO42- |
下列指定物质的个数比不为1:1的是( )
| A、D2O中质子数与中子数 |
| B、Na2O2中的阴,阳离子数 |
| C、SO2与氯水反应生成两种强酸的反应中,氧化剂与还原剂 |
| D、沸水时纯水中H+与OH- |
下列说法正确的是( )
| A、硅和石墨都是重要的半导体材料 |
| B、SO2、NO2、CO2都会导致酸雨的形成 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理不同 |
| D、氢能是清洁能源,工业上用电解水法制大量氢气符合节能减排理念 |