工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物--合金.这是制取合金的常用方法之一.根据下表数据判断,不宜用上述方法制取合金的是( )
| 金属 | Na | Al | Cu | Fe |
| 熔点(℃) | 97.81 | 660 | 1083 | 1535 |
| 沸点(℃) | 883 | 2200 | 2595 | 3000 |
| A、Fe-Cu合金 |
| B、Cu-Al合金 |
| C、Al-Na合金 |
| D、Cu-Na合金 |
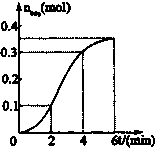 已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )
已知CaCO3与稀盐酸的反应为放热反应,取一定量的CaCO3与稀盐酸进行实验,生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )| A、反应开始后2~4分钟内平均反应速率最大 |
| B、反应刚开始时反应速率较小,然后逐渐增大 |
| C、反应前阶段速率逐渐增大,是因为反应放热,使反应速率加快 |
| D、生成物CaCl2、CO2和H2O的总能量比反应物CaCO3和盐酸的总能量高 |
下列每组中各有两对物质,它们都能用分液漏斗分离的是( )
| A、溴苯和水,酒精和水 |
| B、四氯化碳和水,溴苯和己烷 |
| C、豆油和水,苯和溴苯 |
| D、汽油和水,己烷和水 |
意大利科学家最近合成了一种新型的氧分子,其化学式为O4,对其说法正确的是( )
| A、O4是一种化合物 |
| B、O4是由O2组成的混合物 |
| C、O4是一种单质 |
| D、一个O4分子由2个O2分子构成 |
下列提纯物质的方法正确的是( )
| A、除去HNO3溶液中的少量H2SO4,可加适量BaCl2溶液 |
| B、除去铝粉中的少量铁粉,可加适量盐酸 |
| C、除去FeCl3溶液中的少量FeCl2,可加适量氯水 |
| D、除去NH4NO3固体中的少量NH4Cl,可加适量NaOH溶液 |
下列有关氕(H)、氘(D)、氚(T)的说法正确的是( )
| A、是三种不同的元素 |
| B、H元素平均的相对原子质量=(1+2+3)÷3 |
| C、通常我们把氢的相对原子质量当1来计算,这是以氕的相对原子质量为标准计算的 |
| D、自然界中所有含氢物质中都含有氕、氘、氚三种核素 |
下列变化过程中,△S<0的是( )
| A、干冰升华 |
| B、CaCO3(s)分解为CaO(s)和CO2(g) |
| C、NH3(g)与HCl(g)反应生成NH4Cl(s) |
| D、氯化钠溶于水中 |
向含有NaBr和KI的混合溶液中通入氯气充分反应后将溶液蒸干,并灼烧所得物质,最后剩余的固体可能是( )
| A、NaCl和KI |
| B、NaCl和I2 |
| C、KCl和NaBr |
| D、KCl和I2 |
在MgCl2和AlCl3的混合液中,Cl-的物质的量为0.7mol.向该溶液中加入100mL 8mol/L的KOH溶液,使之充分反应.若反应前Al3+的物质的量与混合溶液中离子总物质的量的比值为x.以下说法正确的是( )
A、若反应前Al3+的物质的量为a mol,则a=
| ||
| B、只有当x为0.1时,加入87.5mL的KOH,溶液中的阳离子恰好完全沉淀 | ||
| C、当100mL KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的值为0.2 | ||
| D、x的取值范围是0<x≤0.25 |