0 124794 124802 124808 124812 124818 124820 124824 124830 124832 124838 124844 124848 124850 124854 124860 124862 124868 124872 124874 124878 124880 124884 124886 124888 124889 124890 124892 124893 124894 124896 124898 124902 124904 124908 124910 124914 124920 124922 124928 124932 124934 124938 124944 124950 124952 124958 124962 124964 124970 124974 124980 124988 203614
 cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。
cC(g) + dD(g) ,反应时间与C%(产物C的体积分数)函数关系如图所示。A图表示的是温度不同的曲线,B图表示压强不同的曲线,C图表示使用催化剂和不使用催化剂时的反应曲线。

 CO(g) + H2O(g),
CO(g) + H2O(g), CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):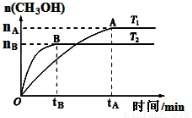
 2H2O + 。
2H2O + 。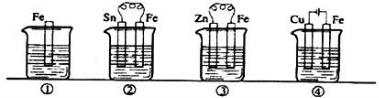
 O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol