某温度下,某容积恒定的密闭容器中发生如下可逆反应
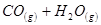

 △H
△H
当反应达平衡时,测得容器中各物质均为 ,欲使
,欲使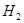 的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
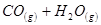

 △H
△H
当反应达平衡时,测得容器中各物质均为
 ,欲使
,欲使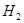 的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是| A.升高温度 | B.再加入 |
C.再加入 和 和 | D.再加入 和 和 |
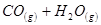

 △H
△H
 ,欲使
,欲使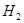 的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是
的平衡浓度增大一倍,在其它条件不变时,下列措施可以采用的是| A.升高温度 | B.再加入 |
C.再加入 和 和 | D.再加入 和 和 |