一定温度下,可逆反应A(气)+3B(气) 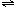 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是
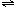 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是| A.单位时间生成n摩尔A,同时生成3n摩尔B | B. A,B,C的浓度不再变化 |
| C. A,B,C的分子数之比为1:3:2 | D.V正=V逆=0 |
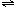 2C(气)达到平衡的标志是
2C(气)达到平衡的标志是| A.单位时间生成n摩尔A,同时生成3n摩尔B | B. A,B,C的浓度不再变化 |
| C. A,B,C的分子数之比为1:3:2 | D.V正=V逆=0 |