0 109230 109238 109244 109248 109254 109256 109260 109266 109268 109274 109280 109284 109286 109290 109296 109298 109304 109308 109310 109314 109316 109320 109322 109324 109325 109326 109328 109329 109330 109332 109334 109338 109340 109344 109346 109350 109356 109358 109364 109368 109370 109374 109380 109386 109388 109394 109398 109400 109406 109410 109416 109424 203614
 H固体
H固体 用蒸馏水洗涤干净,并用各待盛溶液润洗。
用蒸馏水洗涤干净,并用各待盛溶液润洗。
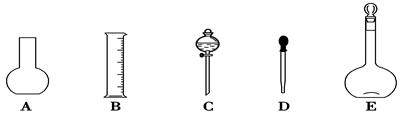
 次,洗涤液也转移至容量瓶
次,洗涤液也转移至容量瓶 托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1 (填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol·L-1;溶解NaOH后在未降至室温时,立即将N
托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol·L-1 (填“大于”“等于”或“小于”,下同);若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol·L-1;溶解NaOH后在未降至室温时,立即将N aOH溶液转移至容量瓶定容,则所得溶液浓度_______ 0.1 mol·L-1。
aOH溶液转移至容量瓶定容,则所得溶液浓度_______ 0.1 mol·L-1。
 Cl 2 + 5Cl 2↑ + 8H2O
Cl 2 + 5Cl 2↑ + 8H2O