0 108259 108267 108273 108277 108283 108285 108289 108295 108297 108303 108309 108313 108315 108319 108325 108327 108333 108337 108339 108343 108345 108349 108351 108353 108354 108355 108357 108358 108359 108361 108363 108367 108369 108373 108375 108379 108385 108387 108393 108397 108399 108403 108409 108415 108417 108423 108427 108429 108435 108439 108445 108453 203614

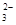 =2I-+S4O
=2I-+S4O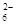 ,当蓝色褪去H半分钟不变色时到达滴定终点。实验数据如下表:
,当蓝色褪去H半分钟不变色时到达滴定终点。实验数据如下表:



