0 108171 108179 108185 108189 108195 108197 108201 108207 108209 108215 108221 108225 108227 108231 108237 108239 108245 108249 108251 108255 108257 108261 108263 108265 108266 108267 108269 108270 108271 108273 108275 108279 108281 108285 108287 108291 108297 108299 108305 108309 108311 108315 108321 108327 108329 108335 108339 108341 108347 108351 108357 108365 203614
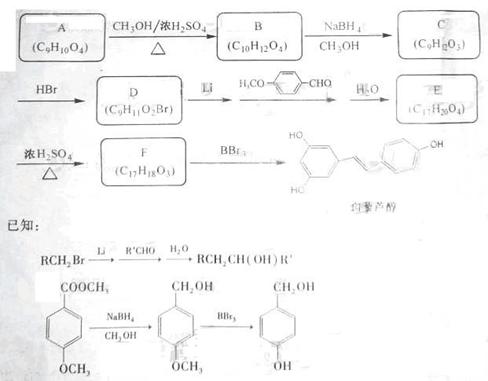
 B反应的化学方程式_______
B反应的化学方程式_______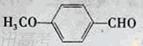 有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:______。
有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式:______。 (X为卤原子,R为取代基)
(X为卤原子,R为取代基)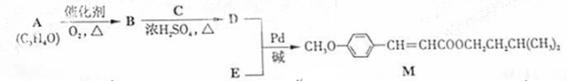

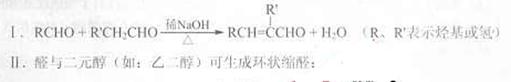
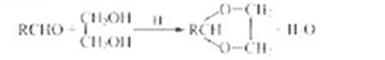
 种峰,A的名称是
种峰,A的名称是 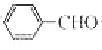 合成B的化学方程式是
合成B的化学方程式是 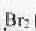 的
的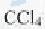 溶液褪色,N由A经反应1~3合成。
溶液褪色,N由A经反应1~3合成。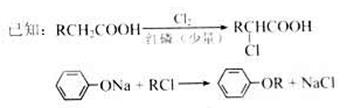

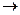 C的反应方程式:
C的反应方程式: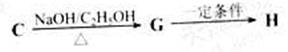
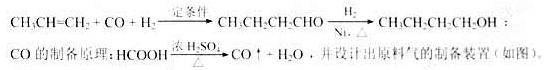
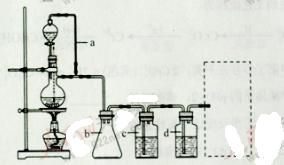
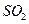 ,
,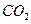 及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________________(填序号)
及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________________(填序号)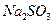 溶液 ②酸性
溶液 ②酸性 溶液 ③石灰水
溶液 ③石灰水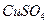 ⑤品红溶液
⑤品红溶液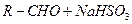 (饱和)→
(饱和)→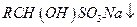 ;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线:
;②沸点:乙醚34°C,1-丁醇118°C,并设计出如下提纯路线: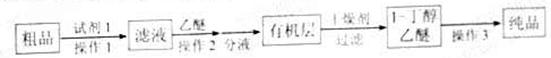
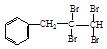 与NaOH的水溶液共热的化学方程式为: ;
与NaOH的水溶液共热的化学方程式为: ;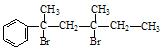 与NaOH的醇溶液共热可以生成 种稳定的二烯烃。
与NaOH的醇溶液共热可以生成 种稳定的二烯烃。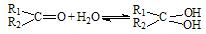 ;这是一个可逆反应,平衡状态(平衡的位置)决定于醛酮的结构。若
;这是一个可逆反应,平衡状态(平衡的位置)决定于醛酮的结构。若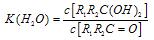 为醛酮的水合平衡常数,其值越大则对应的醛酮水合物越稳定。下表是部分醛、酮的水合平衡常数:
为醛酮的水合平衡常数,其值越大则对应的醛酮水合物越稳定。下表是部分醛、酮的水合平衡常数:
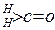
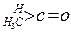
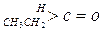
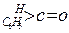
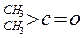
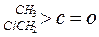
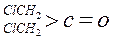
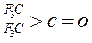
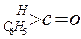 有以下两种方法:
有以下两种方法: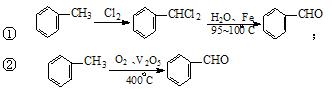


 ,则杜鹃素的分为 。
,则杜鹃素的分为 。 ,则杜鹃素分子中一Y的名称为 。
,则杜鹃素分子中一Y的名称为 。
 H
H CH2+HBr
CH2+HBr CH3CH2CH2Br
CH3CH2CH2Br B的化学方程式为
B的化学方程式为  。
。 构体有 种(对羟基苯甲酸乙酯自身除外)。
构体有 种(对羟基苯甲酸乙酯自身除外)。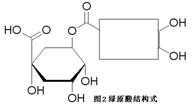
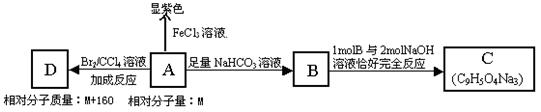

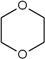 )。
)。 稍有香味,主要用作溶剂、乳化剂、去垢剂等,其分子式为 。
稍有香味,主要用作溶剂、乳化剂、去垢剂等,其分子式为 。