0 102535 102543 102549 102553 102559 102561 102565 102571 102573 102579 102585 102589 102591 102595 102601 102603 102609 102613 102615 102619 102621 102625 102627 102629 102630 102631 102633 102634 102635 102637 102639 102643 102645 102649 102651 102655 102661 102663 102669 102673 102675 102679 102685 102691 102693 102699 102703 102705 102711 102715 102721 102729 203614
 中的①~⑩中元素,用元素符号或化学式填空回答:
中的①~⑩中元素,用元素符号或化学式填空回答: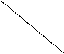 族
族 过程 。
过程 。

 ,呈两性的是 ;
,呈两性的是 ; 镁是制造汽车、飞机、
镁是制造汽车、飞机、 火箭的重要材料。写出工业上电解熔融
火箭的重要材料。写出工业上电解熔融 。
。 子方程式_______________________________,______________________。
子方程式_______________________________,______________________。
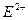 B.R+ C.T3+ D.
B.R+ C.T3+ D.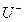
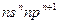 ,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题:
,A原子的最外层电子数等于其电子层数。D和E可以形成原子个数比为1:1和1:2的两种离子化合物,且D原子的2p能级上有两个未成对电子,试回答下列问题: 学式,下同);第一电离能从大到小的顺序是
学式,下同);第一电离能从大到小的顺序是  _____________,D2-的结构示意图___________。A、D可形成多种化合物,其中一种是氧化剂,其水溶液有弱酸性,写出该化合物的结构式________________,分子中含有_____________________键(填“极性”或“非极性”,下同)是__________分子。
_____________,D2-的结构示意图___________。A、D可形成多种化合物,其中一种是氧化剂,其水溶液有弱酸性,写出该化合物的结构式________________,分子中含有_____________________键(填“极性”或“非极性”,下同)是__________分子。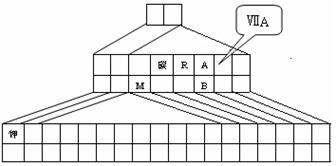
 中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。该离子可能具有的化学性质是_________,依据是_______________________________。
中,B元素呈现最高价,B原子位于由A原子组成的四面体的中心,且所有原子的最外层电子均满足8电子结构。该离子可能具有的化学性质是_________,依据是_______________________________。
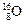 、
、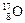 、
、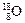 三种核素,氢元素有
三种核素,氢元素有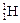 、
、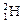 、
、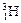 三种核素。
三种核素。 分子
分子