根据已知条件,对物质的性质强弱判断不正确的是
A.已知 ,说明非金属性:碳>硅 ,说明非金属性:碳>硅 |
B.已知相同条件下气态氢化物的稳定性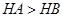 ,说明还原性: ,说明还原性: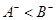 |
C.已知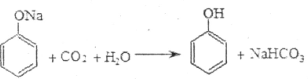 ,说明酸性:碳酸>苯酚 ,说明酸性:碳酸>苯酚 |
D.已知相同物质的量浓度的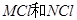 两溶液中 两溶液中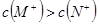 ,说明碱性: ,说明碱性: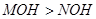 |
A.已知 ,说明非金属性:碳>硅 ,说明非金属性:碳>硅 |
B.已知相同条件下气态氢化物的稳定性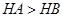 ,说明还原性: ,说明还原性: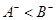 |
C.已知 ,说明酸性:碳酸>苯酚 ,说明酸性:碳酸>苯酚 |
D.已知相同物质的量浓度的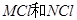 两溶液中 两溶液中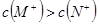 ,说明碱性: ,说明碱性: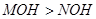 |