0 100189 100197 100203 100207 100213 100215 100219 100225 100227 100233 100239 100243 100245 100249 100255 100257 100263 100267 100269 100273 100275 100279 100281 100283 100284 100285 100287 100288 100289 100291 100293 100297 100299 100303 100305 100309 100315 100317 100323 100327 100329 100333 100339 100345 100347 100353 100357 100359 100365 100369 100375 100383 203614
 题:
题: 2-。
2-。 20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为: ;向此反应后的溶液中滴加
20mLpH=2的NaHSO4溶液逐滴加入到20mL 0.1 mol·L-1Na2CO3溶液中,溶液中发生反应的离子方程式为: ;向此反应后的溶液中滴加 H++OH- KW=10-14
H++OH- KW=10-14  H++CH3COO--> Ka=1.8×10-5
H++CH3COO--> Ka=1.8×10-5
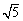 =2.2)
=2.2) 溶液中: HCO3-、 Ag+、 Fe3+、 Cl-
溶液中: HCO3-、 Ag+、 Fe3+、 Cl-
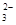 、NO
、NO
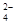 、
、