��Ŀ����
(NH4)2PtCl6�������ȷֽ⣬���ɵ������Ȼ��⡢�Ȼ�狀ͽ��������ڴ˷ֽⷴӦ�У����������뻹ԭ��������ʵ���֮����
��A��2:3 B��3:2 C��4:3 D��1:3
�����������ݷ�Ӧǰ���Ԫ�صĻ��ϼ۱仯���жϣ�NԪ���ɣ�3�����ߵ�0�����������������ÿ����1mol����ת��6mol���ӡ�Pt�Ļ��ϼ��ɣ�4�۽��͵�0�ۣ�����Pt�ǻ�ԭ������ݵ�ʧ�����غ��֪���ɲ������ʵ�����![]() ��������������ͻ�ԭ��������ʵ���֮����2:3��ѡ��A��ȷ����ѡA��
��������������ͻ�ԭ��������ʵ���֮����2:3��ѡ��A��ȷ����ѡA��
A

(NH4)2PtCl6�������ȷֽ⣬���ɵ������Ȼ��⡢�Ȼ�狀ͽ��������ڴ˷ֽⷴӦ�У����������뻹ԭ��������ʵ���֮����
| A��2��3 | B��3��2 |
| C��4��3 | D��1��3 |
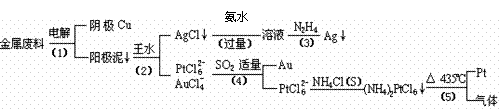
��10�֣��Ӻ�����п����Ͳ��Ľ���ͭ��������ȡ����������һ�ֹ������£��߿���Դ��
����ˮ��Ũ������Ũ����Ļ����߿���Դ��
 �߿���Դ��
�߿���Դ��
�߿���
�������Ϲ��ջش��������⣺
��1�����ʱ����ͭ��������Ϊ��������ͭΪ������CuSO4��ҺΪ���Һ��д�������缫��Ӧ����ʽ�� ��
��2���£�N2H4���ǻ�����䳣�õ�һ��Һ��ȼ�ϣ�����ȫȼ��ʱ������������Ⱦ�����塣��֪���ֹ��ۼ��ļ����������±���
��ѧ�� | N-N | O=O | N��N | O-H | N-H |
����/kJ?mol-1 | 193 | 499 | 941 | 460 | 393 |
������ȫȼ��ʱ���Ȼ�ѧ����ʽΪ�� ��
��3��д�����裨4�������ӷ�Ӧ����ʽ�� ��
��4�����Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��Au + 6HNO3��Ũ��= Au(NO3)3 + 3NO2��+ 3H2O�����÷�Ӧ��ƽ�ⳣ����С�����Խ��Ũ���Ἰ������Ӧ������ȴ����������ˮ���Լ�Ҫ����ԭ�� ��
��5����֪������(NH4)2PtCl6��KspԼΪ9��10��6�����裨4��������Һ��PtCl62��Ũ��Ϊ1��10��4mol?L- 1����Ҫ��1 m3�ĸ���Һ�п�ʼ����(NH4)2PtCl6�������������NH4Cl���������Ϊ kg��������Һ����ı仯���Բ��ƣ�