题目内容
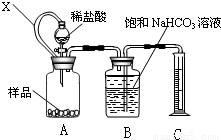
(10分)为测定某种胃药中CaCO3含量,化学兴趣小组同学设计了以下两种方案(药片 中的其它成分与盐酸和NaOH均不反应,请回答有关问题:
中的其它成分与盐酸和NaOH均不反应,请回答有关问题:
(1)方案一:用右侧装置测量一定量样品与足量稀盐酸反应生成CO2的体积计算CaCO3的含量;装置中连通管X的作用是 。
(2)方案二:用滴定法测定,有以下几步操作:
A.配制0.1mol/LHC1溶液和0.100 mol/LNaOH溶液
B.取一粒药片(0. 100g),研碎后加入20mL蒸馏水
C.以酚酞为指示剂,用0.100 mol/LNaOH溶液滴定,用去体积为VmL达到终点
D.用酸式滴定管加入25ml 0.1mol/LHC1溶液,充分反应
 ①滴定过程的正确操作顺序为 (填字母)。
①滴定过程的正确操作顺序为 (填字母)。
滴定终点的判断依据是 。
②若需重复滴定4次,配制0.1mol/LHC1溶液需选用右图所示仪器中的 (填字母)。
③经测定,每次消耗NaOH溶液体积的平均值为13.00ml,则该胃药中CaCO3的质量分数为 ,
④与方案一相比,方案二的主要优点是:除了滴定法所需样品和试剂量少之外,还有 。
(1)使广口瓶与分液漏斗内气体压强相同,便于稀盐酸顺利滴入。 (1分)
(2)①ABDC或BADC(2分);
当最后一滴氢氧化钠溶液时,溶液显(浅)红色且半分钟内不改变。(2分)
②CD或CDE(2分)
③60.0%(2分)
④实验测定结果误差小(1分)

 新思维寒假作业系列答案
新思维寒假作业系列答案
| |||||||||||||||||||
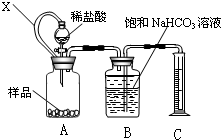 某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
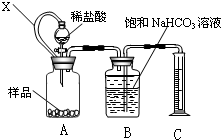 某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题: