题目内容
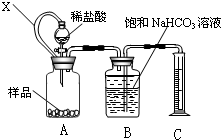 某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
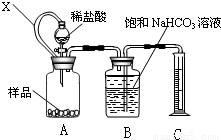
某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:(1)甲同学拟用右图装置测量样品与足量稀盐酸反应生成CO2的体积,来分析CaCO3的含量.则①X的作用是
使广口瓶内与分液漏斗内气体压强相等,便于溶液顺利流下
使广口瓶内与分液漏斗内气体压强相等,便于溶液顺利流下
②B中不可改用饱和Na2CO3溶液,用离子方程式说明理由
CO32-+CO2+H2O=HCO3-
CO32-+CO2+H2O=HCO3-
(2)乙同学拟用以下操作测定样品中CaCO3含量:
A.配制0.100mol/L HCl溶液和0.100mol/L NaOH溶液
B.取一粒药片(0.100g),研碎后加入20mL蒸馏水
C.加入30mL 0.100mol/L 的盐酸,充分反应
D.用0.100mol/L NaOH溶液中和过量的盐酸至中性,共消耗NaOH溶液18.00mL
试回答下列问题:
①配制0.100mol/L HCl溶液100mL需要的玻璃仪器是
100mL容量瓶、烧杯、胶头滴管、玻璃棒
100mL容量瓶、烧杯、胶头滴管、玻璃棒
②该胃药中CaCO3的质量分数是
60%
60%
(3)甲同学将实验中获得的17.92mL CO2 (标准状况)通入10mL 0.100mol/L NaOH溶液中,判断所得溶液的溶质是
Na2CO3、NaHCO3
Na2CO3、NaHCO3
(填化学式)分析:(1)①装置A中连通管X能使分液漏斗和广口瓶中的压强保持一致,使盐酸顺利流下;
②碳酸钠溶液能够和二氧化碳反应生成碳酸氢钠,消耗了二氧化碳;
(2)①根据配制一定物质的量浓度的溶液步骤选择用到的仪器;
②反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为18.00 mL,则与碳酸钙反应的盐酸为30.00mL-18.00 mL=12.00 mL.根据反应:CaCO3+2HCl=CaCl2+H2O+CO2↑计算碳酸钙的质量,再根据质量分数定义计算;
(3)计算出二氧化碳的物质的量和氢氧化钠的物质的量,然后根据二者物质的量关系判断溶液中溶质的组成.
②碳酸钠溶液能够和二氧化碳反应生成碳酸氢钠,消耗了二氧化碳;
(2)①根据配制一定物质的量浓度的溶液步骤选择用到的仪器;
②反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为18.00 mL,则与碳酸钙反应的盐酸为30.00mL-18.00 mL=12.00 mL.根据反应:CaCO3+2HCl=CaCl2+H2O+CO2↑计算碳酸钙的质量,再根据质量分数定义计算;
(3)计算出二氧化碳的物质的量和氢氧化钠的物质的量,然后根据二者物质的量关系判断溶液中溶质的组成.
解答:解:(1)①连通管X能使漏斗和广口瓶中的压强保持一致,使盐酸顺利流下,故答案为:使广口瓶内与分液漏斗内气体压强相等,便于溶液顺利流下;
②若用碳酸钠溶液,溶液中会发生反应:CO32-+CO2+H2O=HCO3-,导致生成的二氧化碳被消耗,测定结果偏小,故答案为:CO32-+CO2+H2O=HCO3-;
(2)①配制0.100mol/L HCl溶液100mL需要的玻璃仪器有100mL容量瓶、烧杯、胶头滴管、玻璃棒,故答案为:100mL容量瓶、烧杯、胶头滴管、玻璃棒;
②反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为18.00 mL,则与碳酸钙反应的盐酸为30.00mL-18.00 mL=12.00 mL.根据反应:CaCO3+2HCl=CaCl2+H2O+CO2↑可知,100g:2mol=m(CaCO3):0.100 mol/L×0.012L,解得:m=0.06 g,碳酸钙的质量分数为
×100%=60%,故答案为:60%;
(3)标况下,17.92mL CO2 的物质的量是
×10-3mol=0.0008mol,10mL0.100mol/L NaOH溶液中含有氢氧根离子的物质的量是0.01L×0.100mol/L=0.001mol,
根据关系式:CO2~Na2CO3~2OH-、CO2~NaHCO3~OH-,完全生成碳酸钠,需要消耗氢氧根离子0.0008mol×2=0.0016mol>0.001mol;完全生成碳酸氢钠,需要消耗氢氧根离子的物质的量是:0.0008mol<0.001mol,氢氧根离子有剩余,所以溶液中溶质是碳酸钠和碳酸氢钠的化合物,
故答案为:Na2CO3、NaHCO3.
②若用碳酸钠溶液,溶液中会发生反应:CO32-+CO2+H2O=HCO3-,导致生成的二氧化碳被消耗,测定结果偏小,故答案为:CO32-+CO2+H2O=HCO3-;
(2)①配制0.100mol/L HCl溶液100mL需要的玻璃仪器有100mL容量瓶、烧杯、胶头滴管、玻璃棒,故答案为:100mL容量瓶、烧杯、胶头滴管、玻璃棒;
②反应所用盐酸与氢氧化钠溶液的浓度相等,氢氧化钠溶液的体积为18.00 mL,则与碳酸钙反应的盐酸为30.00mL-18.00 mL=12.00 mL.根据反应:CaCO3+2HCl=CaCl2+H2O+CO2↑可知,100g:2mol=m(CaCO3):0.100 mol/L×0.012L,解得:m=0.06 g,碳酸钙的质量分数为
| 0.06g |
| 0.1g |
(3)标况下,17.92mL CO2 的物质的量是
| 17.92 |
| 22.4 |
根据关系式:CO2~Na2CO3~2OH-、CO2~NaHCO3~OH-,完全生成碳酸钠,需要消耗氢氧根离子0.0008mol×2=0.0016mol>0.001mol;完全生成碳酸氢钠,需要消耗氢氧根离子的物质的量是:0.0008mol<0.001mol,氢氧根离子有剩余,所以溶液中溶质是碳酸钠和碳酸氢钠的化合物,
故答案为:Na2CO3、NaHCO3.
点评:本题考查对实验原理的理解与实验操作评价、物质含量测定、滴定原理利用,化学计算等,难度中等,理解实验原理是关键,是对所学知识的综合运用,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力,学习中全面把握基础知识

练习册系列答案
相关题目
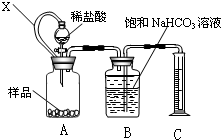 某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题:
某种胃药中抗酸剂为CaCO3.甲、乙两同学为测定其中CaCO3含量,分别设计以下两种方案(药片中的其它成分与HCl和NaOH溶液均不反应).请回答下列有关问题: