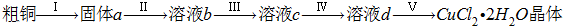题目内容
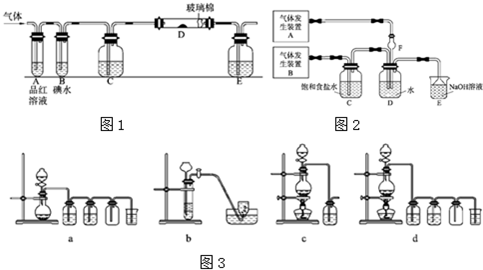
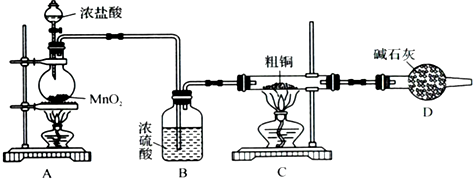
如下图是实验室制备SO2并验证SO2某些性质的装置图。试回答:

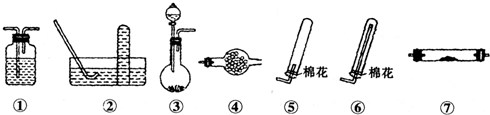
(1)⑥中发生的化学反应方程式为____________________________。
(2)⑤的作用是________________________________,反应的离子方程式为 __________________________。
(3)填表格
(2)⑤的作用是________________________________,反应的离子方程式为 __________________________。
(3)填表格

(1)Na2SO3+H2SO4===Na2SO4+H2O+SO2↑
(2)吸收过量的SO2,防 止污染环境;SO2+2OH-===SO32-+H2O
(3)
(2)吸收过量的SO2,防 止污染环境;SO2+2OH-===SO32-+H2O
(3)


练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目