题目内容
16.如图为“铁链”图案,根据铁链上物质的分类依据,在M处应填入的物质是( )
| A. | CaCl2 | B. | Cl2O | C. | Cl2 | D. | NaClO3 |
分析 根据“铁链”图案可知铁链上物质中氯元素的化合价逐渐递增,据此分析.
解答 解:由“铁链”图案可知铁链上物质中氯元素的化合价逐渐递增,由于HCl中氯元素为-1价,而HClO中氯元素为+1价,故M中填入的物质中氯元素应为0价,即为氯气单质,故选C.
点评 本题考查了根据图示来分析规律从而确定应填入的物质,根据图示来分析出规律是解题的关键,难度不大.

练习册系列答案
相关题目
6.某大学研制成功的新型碱性聚合物电解质燃料电池,有望大幅降低燃料电池汽车的造价.该甲醇燃料电池在NaOH介质中的反应为2CH3OH+3O2+4NaOH═2Na2CO3+6H2O,已知电池的效率与反应速率成正比.不同条件下用不同物质表示的反应速率如下,其中对应的电池效率最高的是( )
| A. | v(CH3OH)=0.3 mol•(L•min)-1 | B. | v(O2)=0.4 mol•(L•min)-1 | ||
| C. | v(NaOH)=0.5 mol•(L•min)-1 | D. | v(Na2CO3)=0.01 mol•(L•s)-1 |
7.某研究性学习小组利用下列有关装置对SO2的性质及空气中SO2的含量进行探究(装置的气密性已检查):
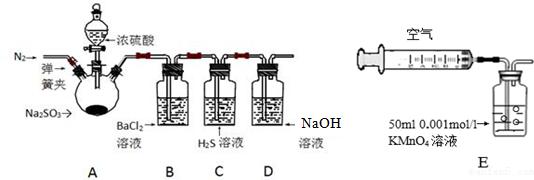
(1)装置A中反应的化学方程式是Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是排除装置中氧气对实验的干扰.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀BaSO3(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有氧化 性.
(5)装置D的作用是吸收SO2尾气,防止污染空气.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
(7)另一小组利用装置E进行实验:SO2性质实验之后,用注射器对实验室内空气进行取样.并向装置E中共注入V mL(已折算为标况下体积)的空气,当溶液刚好褪色时,停止实验.请计算该空气中SO2的体积分数(用含V的代数式表示)$\frac{2.8}{V}$.

(1)装置A中反应的化学方程式是Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O.
(2)滴加浓硫酸之前,打开弹簧夹,通入一段时间N2,再关闭弹簧夹.此操作的目的是排除装置中氧气对实验的干扰.
(3)实验过程装置B中没有明显变化.实验结束取下装置B,从中分别取少量溶液于两支洁净试管中.向第1支试管中滴加适量氨水出现白色沉淀BaSO3(填化学式);向第2支试管中滴加适量新制氯水,仍然出现白色沉淀,该反应的离子方程式是Ba2++SO2+Cl2+2H2O=BaSO4↓+4H++2Cl-.
(4)装置C中的溶液中出现淡黄色浑浊,该实验证明SO2具有氧化 性.
(5)装置D的作用是吸收SO2尾气,防止污染空气.
(6)实验后,测定装置D中溶液呈碱性.溶液为什么呈碱性呢?大家有两种不同的假设:①是生成的Na2SO3水解;②是氢氧化钠剩余.请设计实验方案证明哪种假设成立.可任选下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸
| 实验步骤 | 实验操作 | 预期现象与结论 |
| 1 | 取少量溶液于试管中,滴入几滴酚酞 | 溶液变红 |
| 2 |
4.关于炔烃的描述中正确的是( )
| A. | 分子组成符合CnH2n-2通式的链烃一定是炔烃 | |
| B. | 炔烃既易发生加成反应,又易发生取代反应 | |
| C. | 炔烃既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 | |
| D. | 炔烃分子里所有的碳原子都在同一条直线上 |
11.X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
如图1所示装置中,甲、乙、丙三个烧杯依次分别盛放250mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加6.4g.常温下各烧杯中溶液的pH与电解时间t的关系图2如下.据此回答下列问题:
(1)M为电源的负极(填写“正”或“负”).电解一段时间后,在e、f两极附近分别滴加酚酞,变红的是e极.
(2)甲烧杯中电极b上发生的电极反应为4OH--4e-=O2↑+2H2O.
(3)乙烧杯电解的总反应离子方程式为2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+;甲烧杯中a、b两极共产生标准状况下3.36L的气体.

如图1所示装置中,甲、乙、丙三个烧杯依次分别盛放250mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加6.4g.常温下各烧杯中溶液的pH与电解时间t的关系图2如下.据此回答下列问题:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42-、OH- |
(2)甲烧杯中电极b上发生的电极反应为4OH--4e-=O2↑+2H2O.
(3)乙烧杯电解的总反应离子方程式为2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+4H+;甲烧杯中a、b两极共产生标准状况下3.36L的气体.

1.下列叙述正确的是( )
| A. | 相对分子质量相同、结构不同的化合物一定互为同分异构体 | |
| B. | 结构对称的烷烃,其一氯代物必定只有一种 | |
| C. | 互为同分异构体的化合物不可能具有相同的结构 | |
| D. | 通式为CnH2n且碳原子数不同的有机物一定互为同系物 |
8.在一种酸性溶液中,可能存在NO3-、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下推测中不正确的是( )
| A. | 一定有I- | B. | 可能含Fe3+ | C. | 可能有Cl- | D. | 不含NO3- |
5.下列哪种物质所含原子数与0.3molH2O2所含原子数相等( )
| A. | 0.6molCaO | B. | 0.2molH2SO4 | C. | 0.15molH3PO4 | D. | 0.4molMgCl2 |
6.下列有关实验操作与结论都正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某钠盐中加入稀盐酸,产生能使澄清石灰水变浑浊的气体 | 说明该盐一定是碳酸盐 |
| B | 向某无色溶液中滴加BaCl2溶液,再滴加过量的稀HNO3,产生白色沉淀 | 该无色溶液中一定有SO42- |
| C | 向某无色溶液中滴加NaOH溶液,加热后,产生是湿润的红色石蕊试纸变蓝的气体 | 说明溶液液中含有NH4+ |
| D | 某无色气体通过灼热的CuO,CuO变为红色 | 该气体一定为氢气 |
| A. | A | B. | B | C. | C | D. | D |