题目内容
【题目】酮洛芬是优质抗炎镇痛药,合成原理如下:
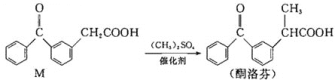
下列说法正确的是( )
A.M和酮洛芬都能发生酯化、卤代和加成反应
B.M和酮洛芬分子中所有碳原子都可能共平面
C.M和酮洛芬在一定条件下最多消耗![]() 的物质的量相等
的物质的量相等
D.M分子中苯环上一氯代物有9种
【答案】A
【解析】
A、苯环上氢能与卤素单质在催化剂作用下发生卤代![]() 取代
取代![]() 反应,苯环与氢气能发生加成反应,苯环之间的碳氧双键与氢气能发生加成反应,羧基与醇羟基在一定条件下能发生酯化反应,故A项正确;
反应,苯环与氢气能发生加成反应,苯环之间的碳氧双键与氢气能发生加成反应,羧基与醇羟基在一定条件下能发生酯化反应,故A项正确;
B、酮洛芬分子右侧链上1个碳原子连接了3个碳原子,这3个碳原子中至少有1个碳原子不能与苯环共平面,故B项错误;
C、若M、酮洛芬的物质的量相等,则它们消耗![]() 最大量相等,没有强调“物质的量相等”,不能判断消耗
最大量相等,没有强调“物质的量相等”,不能判断消耗![]() 的量是否相等,故C项错误;
的量是否相等,故C项错误;
D、M分子中,左边苯环上氢原子有3种![]() 对称结构
对称结构![]() ,右边苯环上氢原子有4种
,右边苯环上氢原子有4种![]() 不对称结构
不对称结构![]() ,故苯环上一氯代物共有7种,故D项错误;
,故苯环上一氯代物共有7种,故D项错误;
故选A。

【题目】锰的用途非常广泛,以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴的碳酸盐及SiO2杂质)为原料生产金属锰的工艺流程如下:
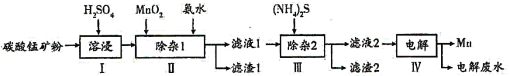
已知25℃时,部分物质的溶度积常数如下:
物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | Fe(OH)3 | MnS | CoS | NiS |
Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.1×10-36 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤I中,为加快溶浸速率,可采取的措施是__________(至少答两条)。
(2)步骤II中,加氨水调节溶液的pH为5.0~6.0,则滤渣1的成分主要为________(填化学式);已知MnO2的作用为氧化剂,“除杂1”中涉及的离子方程式为NH3·H2O+H+=NH4++H2O、_____________、___________。
(3)步骤中,所加(NH4)2S的浓度不宜过大的原因是______________。
(4)滤液2中,c(Co2+):c(Ni2+)=____________。
【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D
【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 易升华 | |
沸点/℃ | 132 | 173 | ---------------------- | -------------------- |
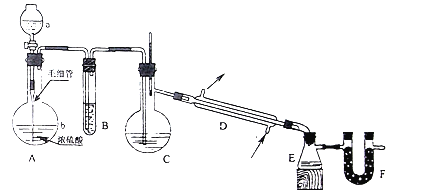
(1)H2还原无水FeCl3制取FeCl2。有关装置如图:
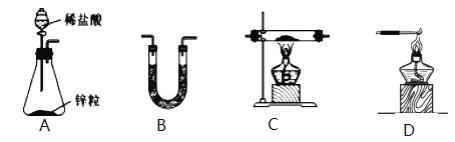
①H2还原无水FeCl3制取FeCl2的化学方程式为_____。
②按气流由左到右的方向,上述仪器的连接顺序为_____。(填字母,装置可多次使用);B中盛放的试剂是_____。
③该制备装置的缺点为_____。
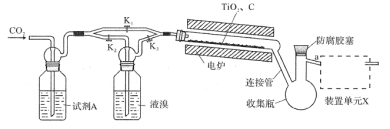
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的作用是_____。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是_____,回收滤液中C6H5C1的操作是_____。
③反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol/L NaOH溶液滴定,终点时消耗NaOH溶液为19.60mL,则氯化铁的转化率为_____。
④为了减少实验误差,在制取无水FeCl2过程中应采取的措施有:_____(写出一点即可)。