题目内容
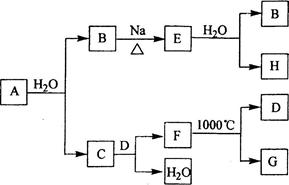
A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示:
请回答下列问题:
(1)A与水反应的化学方程式为______,E与水反应的化学方程式为______;
(2)F的化学式为______,G和D的电子式分别为______和______;
(3)D与H反应可能生成的盐有______ (填化学式);
(4)实际生产中,可由F为原料制备单质A,简述一种制备方法______.
【答案】分析:本题的突破点是A,在自然界存在最广泛的ⅡA族元素中常温下与水反应的是单质Ca,与水反应生成Ca(OH)2和H2,则B是H2,C是Ca(OH)2,E是NaH,H是NaOH,CaCO3受热分解生成CO2和CaO,而CO2恰好与Ca(OH)2反应生成CaCO3和H2O,所以D和G分别是CO2和CaO;Ca作为活泼的金属元素一般只能通过电解法来制备.
解答:解:(1)在自然界存在最广泛的ⅡA族元素中常温下与水反应的是单质Ca,反应的化学方程式为Ca+2H2O═Ca(OH)2+H2↑,在Ca(OH)2和H2中能与金属Na反应的是H2,反应的化学方程式为:H2+2Na═2NaH;所以B是H2,C是Ca(OH)2,E是NaH,NaH与水反应的化学方程式为:NaH+H2O═NaOH+H2↑,所以H是NaOH.
故答案为:Ca+2H2O═Ca(OH)2+H2↑;NaH+H2O═NaOH+H2↑;
(2)由反应条件可知F可能为CaCO3,CaCO3受热分解生成CO2和CaO,而CO2恰好与Ca(OH)2反应生成CaCO3和H2O,所以D和G分别是CO2和CaO;CO2和CaO分别属于共价化合物和离子化合物,分别含有极性共价键和离子键;
故答案为:CaCO3; ;
;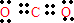
(3)CO2对应的碳酸是二元酸,与NaOH反应时可能会生成两种碳酸盐:Na2CO3和NaHCO3,故答案为:Na2CO3、NaHCO3;
(4)Ca作为活泼的金属元素一般只能通过电解法来制备,可用电解熔融的CaCl2的方法制备.故答案为:将CaCO3与盐酸反应生成CaCl2,然后电解熔融的CaCl2固体制取单质钙.
点评:本题主要考察查常见金属单质及其化合物之间的相互转化,注意框图推断题的突破口,熟悉元素化合物的性质,注意电子式的书写以及金属的冶炼方法.
解答:解:(1)在自然界存在最广泛的ⅡA族元素中常温下与水反应的是单质Ca,反应的化学方程式为Ca+2H2O═Ca(OH)2+H2↑,在Ca(OH)2和H2中能与金属Na反应的是H2,反应的化学方程式为:H2+2Na═2NaH;所以B是H2,C是Ca(OH)2,E是NaH,NaH与水反应的化学方程式为:NaH+H2O═NaOH+H2↑,所以H是NaOH.
故答案为:Ca+2H2O═Ca(OH)2+H2↑;NaH+H2O═NaOH+H2↑;
(2)由反应条件可知F可能为CaCO3,CaCO3受热分解生成CO2和CaO,而CO2恰好与Ca(OH)2反应生成CaCO3和H2O,所以D和G分别是CO2和CaO;CO2和CaO分别属于共价化合物和离子化合物,分别含有极性共价键和离子键;
故答案为:CaCO3;
 ;
;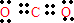
(3)CO2对应的碳酸是二元酸,与NaOH反应时可能会生成两种碳酸盐:Na2CO3和NaHCO3,故答案为:Na2CO3、NaHCO3;
(4)Ca作为活泼的金属元素一般只能通过电解法来制备,可用电解熔融的CaCl2的方法制备.故答案为:将CaCO3与盐酸反应生成CaCl2,然后电解熔融的CaCl2固体制取单质钙.
点评:本题主要考察查常见金属单质及其化合物之间的相互转化,注意框图推断题的突破口,熟悉元素化合物的性质,注意电子式的书写以及金属的冶炼方法.

练习册系列答案
相关题目