题目内容
已知
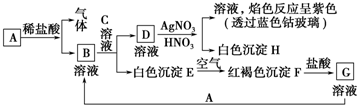
(1)若A为碱性气体,则A→B的化学方程式为______,C→D的化学方程式为______;
(2)若A为空气中含量最多的气体,则A→B的化学方程式为______;
(3)若A为非金属单质,B为导致酸雨的主要气体,则D的浓溶液区别于其稀溶液的特性有:①______性;②______性;
③______性,请用化学方程式举例______.

(1)若A为碱性气体,则A→B的化学方程式为______,C→D的化学方程式为______;
(2)若A为空气中含量最多的气体,则A→B的化学方程式为______;
(3)若A为非金属单质,B为导致酸雨的主要气体,则D的浓溶液区别于其稀溶液的特性有:①______性;②______性;
③______性,请用化学方程式举例______.
(1)若A为碱性气体,则A为NH3,B为NO,C为NO2,D为HNO3,则A→B的化学方程式为4NH3+5O2
4NO+6H2O,C→D的化学方程式为3NO2+H2O=2HNO3+NO,
故答案为:4NH3+5O2
4NO+6H2O;3NO2+H2O=2HNO3+NO;
(2)若A为空气中含量最多的气体,则A为N2,N为NO,则A→B的化学方程式为N2+O2
2NO,
故答案为:N2+O2
2NO;
(3)若A为非金属单质,B为导致酸雨的主要气体,则A为S,B为SO2,C为SO3,D为H2SO4,浓硫酸区别于其稀硫酸溶液的特性有吸水性、脱水性、强氧化性,如碳与浓硫酸反应,其反应方程式为C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,
故答案为:吸水;脱水;强氧化;C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O.
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(2)若A为空气中含量最多的气体,则A为N2,N为NO,则A→B的化学方程式为N2+O2
| ||
故答案为:N2+O2
| ||
(3)若A为非金属单质,B为导致酸雨的主要气体,则A为S,B为SO2,C为SO3,D为H2SO4,浓硫酸区别于其稀硫酸溶液的特性有吸水性、脱水性、强氧化性,如碳与浓硫酸反应,其反应方程式为C+2H2SO4(浓)
| ||
故答案为:吸水;脱水;强氧化;C+2H2SO4(浓)
| ||

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
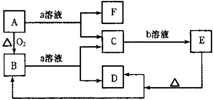 请按要求回答下列问题:
请按要求回答下列问题: